Спектрофотометрия
Спектрофотометрия — метод измерения плотности оптической плотности раствора. При помощи данного метода определяется, как изменяется интенсивность прохождения света через раствор в зависимости от его концентрации. Спектрофотометр используется для измерения различных характеристик раствора на основе абсорбции света.
Измерение плотности оптической плотности производится с помощью спектрофотометра, который обеспечивает точные и повторяемые результаты. Устройство спектрофотометра основано на законе Бугера-Ламберта, согласно которому интенсивность падающего на вещество света экспоненциально убывает с увеличением пути его проникновения в среду. Чем плотнее раствор, тем больше света поглощается, и тем меньше интенсивность излучения, прошедшего через раствор.
С помощью спектрофотометрии можно измерять плотность оптической плотности раствора в разных диапазонах длин волн, что позволяет проводить спектральный анализ вещества. Для этого спектрофотометры используют оптические фильтры или дисперсионные элементы, такие как просвечивающие призмы или решетки, чтобы разделить свет на разные длины волн и измерить его интенсивность на каждой длине волны.
Измерение оптической плотности раствора с помощью спектрофотометрии является важным и удобным методом в аналитической химии, медицине, биологии и других научных областях. Оно позволяет получать количественную информацию о содержании вещества в растворе и определять его свойства на основе взаимодействия со светом.
Описание метода
Оптическая плотность раствора измеряется с использованием специальных приборов, называемых спектрофотометрами. Эти приборы позволяют измерять пропускание света через растворы различной концентрации и определять их оптическую плотность.
Для измерения оптической плотности раствора, сначала необходимо подготовить раствор с известной концентрацией вещества. Затем этот раствор помещается в спектрофотометр, который излучает свет определенной длины волны и измеряет количество света, прошедшего через раствор.
Спектрофотометры обычно используются с двумя кюветами, в которых помещаются растворы для измерения. Одна кювета содержит раствор с известной концентрацией, который служит для калибровки прибора. Вторая кювета содержит раствор с неизвестной концентрацией, оптическую плотность которого необходимо измерить.
Прибор измеряет оптическую плотность раствора путем сравнения пропускания света через обе кюветы. Измеренное пропускание света преобразуется в единицы оптической плотности, такие как абсорбция или оптическая плотность, которые могут использоваться для определения концентрации вещества в растворе.
Измерение оптической плотности раствора имеет широкий спектр применений, включая анализ химических реакций, определение концентрации вещества в растворе, определение молекулярной массы и другие.
Преимущества и ограничения
Оптическая плотность раствора является важной характеристикой, позволяющей определить концентрацию вещества в растворе. Ее измерение осуществляется с помощью специального прибора — спектрофотометра, который позволяет измерить поглощение света в растворе
Преимущества измерения оптической плотности:
- Простота и удобство измерения: для определения оптической плотности не требуется сложной подготовки образца, а также проведения химических реакций.
- Высокая точность: результаты измерений оптической плотности обладают высокой точностью, что позволяет получить достоверную информацию о концентрации вещества в растворе.
- Быстрота измерения: с помощью спектрофотометра можно получить результаты измерений оптической плотности в течение нескольких секунд.
Ограничения измерения оптической плотности:
- Ограниченный диапазон измерений: каждый спектрофотометр имеет свой диапазон измерений, поэтому при измерении оптической плотности необходимо учитывать его ограничения.
- Влияние других параметров: помимо концентрации вещества, оптическая плотность раствора может зависеть от других факторов, таких как температура, давление и pH-значение раствора. Эти параметры могут оказывать влияние на поглощение света и, соответственно, на измерение оптической плотности.
- Необходимость калибровки: перед проведением измерений необходимо провести калибровку спектрофотометра, чтобы установить связь между измеренными значениями оптической плотности и концентрацией вещества в растворе.
В целом, измерение оптической плотности раствора является эффективным методом определения концентрации вещества. Однако для достоверных результатов необходимо учитывать ограничения и проводить измерения с соблюдением требуемых условий.
Методы определения концентрации
Стоит рассмотреть метод градуировочного графика. Для его построения готовят ряд растворов (5-10) с различной концентрацией исследуемого вещества и замеряют их оптическую плотность. По полученным значениям выстраивают график зависимости D от концентрации. График является прямой линией, идущей от начала координат. Он позволяет легко определить концентрацию вещества по результатам проведенных измерений.
Также существует метод добавок. Применяется реже, чем предыдущий, но позволяет проанализировать растворы сложного состава, поскольку учитывает влияние дополнительных компонентов. Суть его состоит в определении оптической плотности среды D x , содержащей определяемое вещество неизвестной концентрации С х, с повторным анализом того же раствора, но с добавлением определенного количества исследуемого компонента (С ст). Величину С х находят, используя расчеты или графики.

Абсорбция
Абсорбция – это процесс поглощения оптической энергии веществом. Она характеризуется оптической плотностью раствора и является важным физическим понятием в оптике и спектроскопии.
Оптическая плотность раствора описывает способность вещества поглощать свет. Она измеряется величиной, называемой коэффициентом поглощения (α) и выражается в см^-1. Чем выше значение коэффициента поглощения, тем больше света раствор способен поглотить.
Величина оптической плотности раствора зависит от концентрации и свойств вещества, растворенного в растворе, а также от длины волны света. Часто оптическую плотность измеряют при помощи спектрофотометра, который определяет изменение интенсивности света после прохождения через раствор.
Значение оптической плотности раствора может быть использовано для определения концентрации вещества в растворе или для исследования его оптических свойств. Такие исследования играют важную роль в различных науках и индустрии, включая химию, медицину, физику и материаловедение.
Описание и формула
Оптическая плотность раствора — это физическая величина, характеризующая меру поглощения светового излучения раствором. Измеряется она в специальных единицах — оптических плотностях (ОП).
Для измерения оптической плотности раствора используются специальные приборы, называемые спектрофотометрами. С помощью спектрофотометра измеряется поглощение света раствором в различных длинах волн. Полученные данные можно представить в виде графика поглощения в зависимости от длины волны.
Оптическая плотность раствора определяется по формуле:
| ОП(λ) | = | log10(I/I) |
|---|
где:
- ОП(λ) — оптическая плотность раствора при определенной длине волны λ;
- I — интенсивность падающего света;
- I — интенсивность прошедшего света.
Величина ОП(λ) позволяет определить степень поглощения света раствором при конкретной длине волны. Чем больше значение оптической плотности, тем больше свет поглощается раствором.
Преобразование абсорбции в оптическую плотность
Оптическая плотность раствора измеряется с использованием спектрофотометра, который позволяет измерить количество света, поглощенного раствором при определенной длине волны.
Абсорбция, или поглощение света, может быть измерена в спектрофотометре посредством сравнения интенсивности падающего света до и после прохождения через раствор. Чем больше света поглощается раствором, тем выше его абсорбция.
Оптическая плотность раствора представляет собой меру концентрации поглощающего вещества в растворе и рассчитывается с использованием закона Бугера. Закон Бугера устанавливает линейную зависимость между абсорбцией (A) и концентрацией поглощающего вещества (c), а также относит показатели абсорбции и оптической плотности на единичное значение пути света (l).
- Оптическая плотность (ОП) раствора может быть рассчитана по формуле: ОП = A / l
- Величина оптической плотности может использоваться для определения концентрации вещества в растворе, используя формулу: c = A / (l * е), где е — коэффициент поглощения.
Преобразование абсорбции в оптическую плотность позволяет получить количественные данные о концентрации поглощающего вещества в растворе и является важным шагом в многих аналитических методах, таких как спектрофотометрия и химический анализ.
Основные закономерности светопоглощения
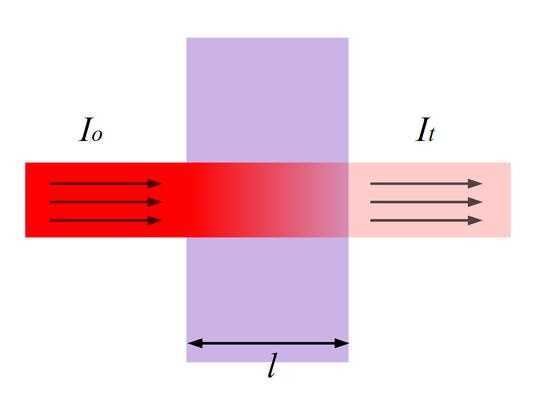
При прохождении через слой вещества (в частном случае раствора) светового потока с интенсивностью 1его интенсивность вследствие поглощения в слое, отражения и рассеяния уменьшается до значения I. Интенсивность падающего светового потока I и светового потока I, прошедшего через раствор, можно определить экспериментально.
Связь между интенсивностями световых потоков I и I устанавливается законом Бугера-Ламберта, согласно которому однородные слои одного и того же вещества одинаковой толщины поглощают одну и ту же долю падающей на них световой энергии (при постоянной концентрации растворенного вещества). Материалистически этот закон выражается уравнением экспоненциальной зависимости:
где е — основание натуральных логарифмов;
к — коэффициент поглощения;
l — толщина поглощающего слоя.
Отношение I/Iназывают пропусканием (Т); его значения могут изменяться от 0 до 1. Часто эту величину выражают в процентах. Если величина Т отнесена к толщине слоя в 1 см, то ее называют коэффициентом пропускания. Поглощение излучения характеризуют оптической плотностью:
Связь между концентрацией поглощающего раствора и его оптической плотностью lg (I/I) выражается законом Бера, согласно которому оптическая плотность раствора прямо пропорциональна концентрации растворенного вещества при постоянной толщине слоя:
где к1 — коэффициент пропорциональности;
С — концентрация растворенного вещества.
Зависимость монохроматического светового потока, прошедшего через слой окрашенного раствора, от интенсивности падающего потока света, концентрации окрашенного вещества и толщины раствора определяется объединенным законом Бугера-Ламбера-Бера, который является основным законом светопоглощения и лежит в основе большинства фотометрических методов анализа.
где к — коэффициент светопоглощения, зависящий от природы растворенного вещества, температуры, растворителя и длины волны света.
Если концентрация С выражена в молях на литр, a l — в сантиметрах, то к представляет собой молярный коэффициент светопоглощения и обозначается Ел. Основной закон светопоглощения в этом случае будет иметь следующий вид:
При соблюдении основного закона светопоглощения оптическая плотность раствора прямо пропорциональна молярному коэффициенту светопоглощения, концентрации поглощающего вещества и толщине слоя раствора:
При графическом изображении зависимость оптической плотности от концентрации (при постоянном значении д) С получается прямая линия. Эта прямая проходит через начало координат при отсутствии поглощения света растворителем и систематических погрешностей (рис. 2.1).
Оптическая плотность — стандартный раствор
Оптические плотности стандартных растворов и раствора реагента ( холостого опыта, содержащего определенный объем добавляемого реагента) измеряют относительно растворителя. Определяют разности значений ДЛ А — А % ( где А и Лр — средние значения при разных концентрациях) и строят график или рассчитывают уравнение зависимости АЛ f ( С) ( см. разд. Этот подход наиболее применим для неустойчивых систем или реагентов и систем, содержащих примеси.
|
Градуировочный график. |
Оптические плотности стандартных растворов и раствора реагента ( холостого опыта, содержащего определенный объем добавляемого реагента) измеряют относительно растворителя. Этот подход наиболее применим для неустойчивых систем или реагентов и систем, содержащих примеси.
Оптические плотности стандартных растворов измеряют на фотоэлектроколориметре, и на основании полученных данных строят калибровочную кривую.
Оптические плотности стандартного раствора известной концентрации и исследуемого раствора измеряют, пользуясь ФЭК-56. Максимальное поглощение ионами дихромата, наблюдается при Я т 400 — 450 ммк.
Оптическую плотность стандартных растворов измеряют через 30 мин и на основании полученных результатов строят калибровочный график.
Оптическую плотность стандартных растворов измеряют через 30 мин, и на основании полученных результатов строят калибровочный график.
Оптическую плотность стандартного раствора определяют сле дующим образом.
Измеряют оптические плотности стандартных растворов с известной концентрацией. По полученным данным строят калибровочный график, откладывая на оси ординат значения оптической плотности, а на оси абсцисс — соответствующие им значения концентрации. Затем измеряют оптическую плотность исследуемых растворов и по графику находят их концентрации. Этот метод наиболее удобен для выполнения серийных определений.
Измеряют оптическую плотность стандартных растворов КМпО4 при 550 и 430 нм и оптическую плотность стандартных растворов К2Сг2О7 при 430 нм.
Измеряют оптическую плотность стандартных растворов по отношению к раствору сравнения ( в порядке возрастания концентраций) в кюветах со слоем толщиной 50 мм с синим светофильтром.
Определяют оптическую плотность стандартных растворов йода с цветным числом от 2 до 25 мг йода на электрофотоколориметре, используя синий светофильтр ( Х 450 — 480 нм) и кювету с расстоянием между рабочими гранями 20 мм. В правый пучок света помещают кювету со стандартным раствором йода, а в левый — кювету с дистиллированной водой.
Ст — оптическая плотность стандартного раствора; Уал — аликвотная часть раствора, взятая для анализа, мл; т — навеска образца, мг.
Значение величины оптической плотности стандартных растворов откладывают по оси ординат, а соответствующую этим значениям массовую концентрацию глюкозы — в мг / см3 — по оси абсцисс.
|
Стандартная шкала для определения теллура. |
Прибор предназначен для измерения оптиче¬ской плотности растворов пределах от 0 до 1,3; большие оптические плотности измеряются менее точно.
Принцип работы фотоэлектроколориметров состоит в сравнении интенсивности потоков света, прошедшего через раствори¬тель (I0) и через исследуемый раствор (I). Внешний вид и оптическая схема ФЭК-56М представлена на рис. 4 и 5.
Рис. 4. Внешний вид фотоэлектроколориметра ФЭК-56М: 1 – источник света (лампа накаливания); 2 – шторка; 3 – кюветное от-деление ; 4 – барабан светофильтров; 5, 6 – левый и правый барабаны; 7 – микроамперметр; 8 , 9 – шкалы для считывания показаний.
Для измерения светопоглощения выбирают спектральную область, в которой чувствительность анализа наиболее высокая. Фо-тоэлектроколориметр ФЭК-56М снабжен кассетой с девятью светофильтрами (табл.8). При выборе светофильтра необходимо знать области поглощения света веществом (его спектр).
Длина волны в максимуме пропускания, нм
Ширина полосы пропускания, нм
Как известно, ощущение цвета возникает в результате воздействия на зрительный нерв электромагнитного излучения с длинами волн 380-760 нм (т. н. видимая часть спектра). Суммарное действие электромагнитных излучений во всем указанном интервале вызывает ощущение белого цвета. При отсутствии в видимой части спектра определенного интервала длин волн возникнет ощущение цветности. Если вещество поглощает луч какого-либо цвета (назовем его спектральным), оно окрашивается в так называемый дополнительный цвет. Именно он возникает в зрительном аппарате, если из белого луча изымается спектральный цвет. Например, если вещество поглощает свет с длиной волны 590 нм (желтый), то оно окрашено в синий цвет (425 нм).
В соответствии с вышесказанным, цвет светофильтра должен являться дополнительным по отношению к окраске раствора (табл.9).
Соотношение окраски растворов и характеристики светофильтров
Поглощаемая длина волны, нм
Длина волны пропускаемого света, нм
Рис. 5. Оптическая схема ФЭК-56М. 1 – источник света; 2 – сменный светофильтр; 3 – призма; 4 – зеркала; 5 – кюветы с рас-творами ; 6 – раздвижные диафрагмы с измерительными барабанами; 7 – фотоэлементы; 8 – усилитель; 9 – микроамперметр. A NAME=» Порядок работы на приборе ФЭК-56М»>
Расчет концентрации светопоглощающих растворов
При работе с приборами, позволяющими непосредственно измерять оптическую плотность D, для расчета концентрации испытуемых растворов можно применять следующие методы.
1. Графический метод, основанный на построении калибровочного графика в координатах оптическая плотность — концентрация.
Для построения калибровочного графика измеряют поглощение серии окрашенных растворов известной, но различной концентрации, оптические плотности которых охватывают требуемый интервал. С этой целью применяют стандартный раствор определяемого вещества. Тщательно отмеряют пипеткой определенные части этого раствора, добавляют к ним соответствующий реагент и соблюдают условия максимального развития окраски (время выдержки, температура). После этого каждый раствор разбавляют в мерной колбе до определенного объема и измеряют поглощение при выбранной длине волны. График зависимости поглощения света от концентрации поглощающего вещества обычно представляет собой прямую линию, тангенс угла наклона которой равен коэффициенту пропускания Т или молярному коэффициенту поглощения E с лямбдой. При построении калибровочного графика результаты измерений вначале наносят в виде 5-8 точек, различающихся по концентрации не менее чем на 30%, а затем проводят прямую линию либо через эти точки, либо как можно ближе к ним. Это ведет к усреднению и уменьшению ошибок, вызванных неточностями приготовления и измерения поглощения стандартных растворов. Фотометрическую реакцию анализируемого образца проводят в тех же условиях, что и для стандартных растворов. Измерив поглощение раствора образца, можно по калибровочному графику определить его концентрацию.
2. Если заранее известно, что испытуемые растворы подчиняются законам поглощения излучений, то приготовляют два раствора — эталонный, концентрация которого Сэ известна, и испытуемый (его концентрация Сх) и определяют их оптические плотности Dэ и Dx. Концентрацию испытуемого раствора вычисляют по формуле:
3. Если заранее известно значение молярного коэффициента поглощения при данной длине волны монохроматического света E с лямбдой, то, зная толщину поглощающего слоя (толщину слоя кюветы), концентрацию испытуемого раствора вычисляют по формуле:
Основной закон светопоглощения
Суть фотометрического определения заключается в двух процессах:
- перевод определяемого вещества в поглощающее электромагнитные колебания соединение;
- замер интенсивности поглощения этих самых колебаний раствором исследуемого вещества.
Изменения в интенсивности потока света, проходящего через светопоглощающее вещество, будут вызываться также потерями света из-за отражения и рассеяния. Чтобы результат был достоверным, проводят параллельные исследования по замеру параметров при той же толщине слоя, в идентичных кюветах, с тем же растворителем. Так снижение интенсивности света зависит главным образом от концентрации раствора.
Уменьшение интенсивности света, пропущенного через раствор, характеризуют коэффициентом светопропускания (также принято называть его пропусканием) Т:
- I — интенсивность света, пропущенного через вещество;
- I — интенсивность падающего пучка света.
Таким образом, пропускание показывает долю непоглощенного светового потока, проходящего через изучаемый раствор. Обратный алгоритм значения пропускания называют оптической плотностью раствора (D): D = (-lgT) = (-lg) * (I / I) = lg * (I / I).
Это уравнение показывает, какие параметры являются главными для исследования. К ним относится длина волны света, толщина кюветы, концентрация раствора и оптическая плотность.
Спектрофотометрические методы анализа
Спектрофотометрия широко применяется для установления связи между спектрами поглощения различных веществ и их химическим строением и составом, а также для количественного определения веществ.
Абсорбционная спектрометрия основана на тех же законах светопоглощения, что и фотоколориметрические методы, однако, в отличие от последних, в ней используется поглощение монохроматического света с очень узким интервалом длин волн (1-2 нм). Это значительно увеличивает чувствительность и точность количественного анализа окрашенных растворов, поглощающих свет в видимой области спектра, а также «бесцветных» для глаза растворов, которые поглощают излучение в ультрафиолетовой (200-400 нм) или ближней инфракрасной области спектра.
Спектрофотометры подразделяются на регистрирующие и нерегистрирующие. В регистрирующих приборах результаты всех измерений автоматически записываются на специальном бланке, имеющем вид сетки.
Нерегистрирующие спектрофотометры обычно включают источник излучения, монохроматор, приемник излучения и отсчетное устройство. Количественные измерения пропускания производятся сравнением сигналов приемника при попеременной установке в световой пучок образца и эталона. При измерениях поглощения светового потока жидкостями обычно пользуются двумя идентичными кюветами, одна из которых заполняется исследуемым раствором, а другая (пустая или наполненная растворителем) играет роль эталона, пропускание которого принимают за 100%, а оптическую плотность считают равной нулю.
К нерегистрирующим спектрофотометрам с кварцевой оптикой относятся модели СФ-4, СФ-4А, СФ-16, обеспечивающие возможность производить измерения, помимо видимой и ближней инфракрасной, также в ультрафиолетовой области спектра.
К нерегистрирующим спектрографам со стеклянной оптикой относится модель СФ-5, используемая для измерений только в видимой и ближней инфракрасной области спектра.
Нерегистрирующие спектрофотометры имеют одинаковую оптическую схему, но несколько различаются электрическими схемами и методикой измерений.
Принципиальная оптическая схема спектрофотометра СФ-16, с пределами измерения оптических плотностей 0-2 и пропускания 100-0, 10-0, 100-90% представлена на рис. 186. Свет от источника 1 попадает на зеркало-конденсор 2, которое направляет пучок лучей на плоское зеркало 3, поворачивающее лучи на 90° и направляющее их на входную щель монохроматора 4. Зеркальный объектив 6 направляет параллельный пучок лучей на призму 5, которая разлагает его в спектр и возвращает его обратно на объектив 6. Луч, прошедший призму под углом близким к углу наименьшего отклонения, попадает на выходную щель 7, расположенную под входной. Поворачивая призму вокруг оси, можно получить на выходе монохроматора лучи различных длин волн. Выходящий из монохроматора пучок света проходит фильтр 8, кювету с исследуемым раствором 9 и попадает на фотоэлемент 10. Фототок, возникающий в фотоэлементе, передается на усилитель постоянного тока. Усиленный ток попадает на милливольтметр.
Спектрофотометр СФ-16 относится к однолучевым приборам, поэтому в процессе измерений на пути потока излучения устанавливаются поочередно «нулевой» и испытуемый образцы. Происходящие при этом изменения интенсивности излучения, падающего на фотоэлемент, вызывают изменение напряжения в системе усилителя, которое компенсируется путем изменения напряжения на потенциометре, связанном с отсчетным устройством.
Включение прибора в сеть производится согласно прилагаемой к нему инструкции, в которой также даются указания относительно техники работы с ним.
Условия проведения исследования
Чтобы фотометрические исследования давали достоверный результат, необходимо соблюдать несколько условий:
- реакция должна заканчиваться быстро и полностью, избирательно и воспроизводимо;
- окраска образующегося вещества должна быть устойчива во времени и не изменяться под действием света;
- исследуемое вещество берут в количестве, которого достаточно для перевода его в аналитическую форму;
- замеры оптической плотности проводят в том интервале длин волн, при котором различие в поглощении исходных реагентов и анализируемого раствора наибольшее;
- светопоглощение раствора сравнения принято считать оптическим нулем.
Производная спектрофотометрия
В производной спектрофотометрии исходные спектры поглощения (нулевого порядка) преобразуются в спектры производных первого, второго и более высокого порядков.
Спектр первой производной представляет собой график зависимости градиента кривой поглощения (скорость изменения оптической плотности от длины волны, dA/dλ) от длины волны.
Спектр второй производной представляет собой график зависимости кривизны спектра поглощения (d2A/dλ2) от длины волны. Вторая производная при любой длине волны связана с концентрацией следующим соотношением:
где:
А– оптическая плотность при длине волны λ;
– удельный показатель поглощения при длине волны λ;
с– концентрация вещества в растворе, в граммах/100 мл;
l– толщина слоя, в сантиметрах.
Производная спектрофотометрия может быть использована как для целей идентификации веществ, так и для их количественного определения в многокомпонентных смесях, а также в тех случаях, когда имеется фоновое поглощение, вызванное присутствием веществ, содержание которых не регламентируется.
Приборы
Используют спектрофотометры, отвечающие указанным выше требованиям и оснащенные аналоговым резистивно-емкостным дифференцирующим модулем или цифровым дифференциатором, или другими средствами получения производных спектров, в соответствии с инструкцией к прибору. Некоторые методы получения спектров второй производной приводят к смещению длин волн относительно исходного спектра, что следует учитывать там, где это необходимо.
Разрешающая способность
Если указано в фармакопейных статьях, записывают спектр второй производной для раствора 0,2 г/л толуола в метаноле, используя метанол в качестве раствора сравнения. На спектре должен присутствовать небольшой отрицательный экстремум, расположенный между двумя большими отрицательными экстремумами при 261 нм и 268 нм, в соответствии с рис. 1. Если нет других указаний в фармакопейных статьях, отношение А/B должно быть не менее 0,2.
Методика
Процедура анализа аналогична применяемой в обычной спектрофотометрии, но вместо оптических плотностей используют производные. Готовят раствор испытуемого образца, настраивают прибор в соответствии с инструкцией производителя и рассчитывают количество определяемого вещества, как указано в фармакопейной статье.
Рисунок 1 – Спектр второй производной раствора толуола (0,2 г/л) в метаноле
Скачать в PDF ОФС.1.2.1.1.0003.15 Спектрофотометрия в УФ и видимой областях
Заключение
Рефрактометрия — метод исследования веществ, основанный на определении показателя преломления (коэффициента рефракции) и некоторых его функций. Этот метод применяется для идентификации химических соединений, количественного и структурного анализа, определения физико-химических параметров веществ. Показатель преломления – это отношение скоростей света в граничащих средах. Для жидкостей и твердых тел показатель преломления определяют, как правило, относительно воздуха, для газов — относительно вакуума. Значения показателя преломления зависят от длины волны света и температуры. Например, показатель преломления при 20 °С для D-линии спектра натрия (589 нм). Часто используют также линии С и F спектра водорода (соответственно 656 и 486 нм). В случае газов необходимо учитывать зависимость показателя преломления от давления (указывать его или приводить данные к нормальному давлению). Анизотропные тела, одно- и двухосные кристаллы характеризуются соответственно двумя экстремальными или тремя значениями показателя преломления. Все задачи, поставленные вначале исследования, решены. Цель курсовой работы достигнута.
Список использованной литературы
1. Минкин В.И., Осипов О.А., Жданов Ю.А. Дипольные моменты в органической химии: М.: Химия, 1968. – 246 с.
2. Боровиков Ю.А. Диюэлектрометрия в органической химии: Киев: Наукова думка, 1987. – 215 с.
3. Бацанов С.С. Структурная рефрактометрия: Изд-во Московского ун-та, 1959. – 223 с.
4. Шишловский А.А. Прикладная физическая оптика,. ФизматГИЗ, 1970. – 822 с.
5. Ляликов Ю.С. Физико–химические методы анализа, М.: Химия, 1964.
6. Барановский В.Ф., Горелкин С.М., Городенцева В.А. Физико – химические методы анализа: М.: Высшая школа, 1972.
7. Рабек Я. Экспериментальные методы в химии полимеров: М.: Мир, 1983. Ч. 1. – 382 с.
8. Новикова Г.Е., Трапезникова О.Н. // Каучук и резина, 1968. – № 8.
9. Пиотровский К.Б., Стерензат Д.Е. // Каучук и резина, 1957. – № 11.
10. Пилипенко А.Т., Пятницкий И.В. Аналитическая химия; М.: Химия, 1990.
11. Практикум по физической химии под ред. Н.К. Воробьева; М.: Химия, 1975. – 367 с.
12. Иоффе Б.В. Рефрактометрические методы анализа в химии; Л.: Химия
13. Уитли П. Определение молекулярной структуры; М.: Мир, 1970.
14. Методические указания. Рефрактометрия. Лабораторная работа № 1. Волгоград. Изд-во ВПИ, 1983. – 14 с.
15. Краткий справочник физико–химических величин под редакцией К.П Мищенко: М.: Химия, 1967.





























