Взаимодействие алюминия с простыми веществами
с кислородом
При контакте абсолютно чистого алюминия с воздухом атомы алюминия, находящиеся в поверхностном слое, мгновенно взаимодействуют с кислородом воздуха и образуют тончайшую, толщиной в несколько десятков атомарных слоев, прочную оксидную пленку состава Al2O3, которая защищает алюминий от дальнейшего окисления. Невозможно и окисление крупных образцов алюминия даже при очень высоких температурах. Тем не менее, мелкодисперсный порошок алюминия довольно легко сгорает в пламени горелки:
4Аl + 3О2 = 2Аl2О3
с галогенами
Алюминий очень энергично реагирует со всеми галогенами. Так, реакция между перемешанными порошками алюминия и йода протекает уже при комнатной температуре после добавления капли воды в качестве катализатора. Уравнение взаимодействия йода с алюминием:
2Al + 3I2 =2AlI3
С бромом, представляющим собой тёмно-бурую жидкость, алюминий также реагирует без нагревания. Образец алюминия достаточно просто внести в жидкий бром: тут же начинается бурная реакция с выделением большого количества тепла и света:
2Al + 3Br2 = 2AlBr3
Реакция между алюминием и хлором протекает при внесении нагретой алюминиевой фольги или мелкодисперсного порошка алюминия в заполненную хлором колбу. Алюминий эффектно сгорает в хлоре в соответствии с уравнением:
2Al + 3Cl2 = 2AlCl3
с серой
При нагревании до 150-200 оС или после поджигания смеси порошкообразных алюминия и серы между ними начинается интенсивная экзотермическая реакция с выделением света:
— сульфид алюминия
При взаимодействии алюминия с азотом при температуре около 800 oC образуется нитрид алюминия:
с углеродом
При температуре около 2000oC алюминий взаимодействует с углеродом и образует карбид (метанид) алюминия, содержащий углерод в степени окисления -4, как в метане.
Ультрафиолетовые детекторы
Хотя кремний чувствителен в первую очередь к видимым длинам волн, кремниевый фотодиод можно оптимизировать для улучшения отклика и в ультрафиолетовом диапазоне. Эти устройства называются кремниевыми ультрафиолетовыми фотодиодами.
Вы, наверное, знакомы с карбидом кремния (SiC). Это набирающий популярный полупроводниковый материал, который в первую очередь ассоциируется с мощными полевыми MOSFET транзисторами, но оказывается, что диоды из SiC отлично подходят для использования в качестве детекторов ультрафиолетового излучения.
Фотодиоды из карбида кремния – это прочные устройства, которые по своей природе чувствительны только к ультрафиолетовому свету в диапазоне от 200 до 400 нм.
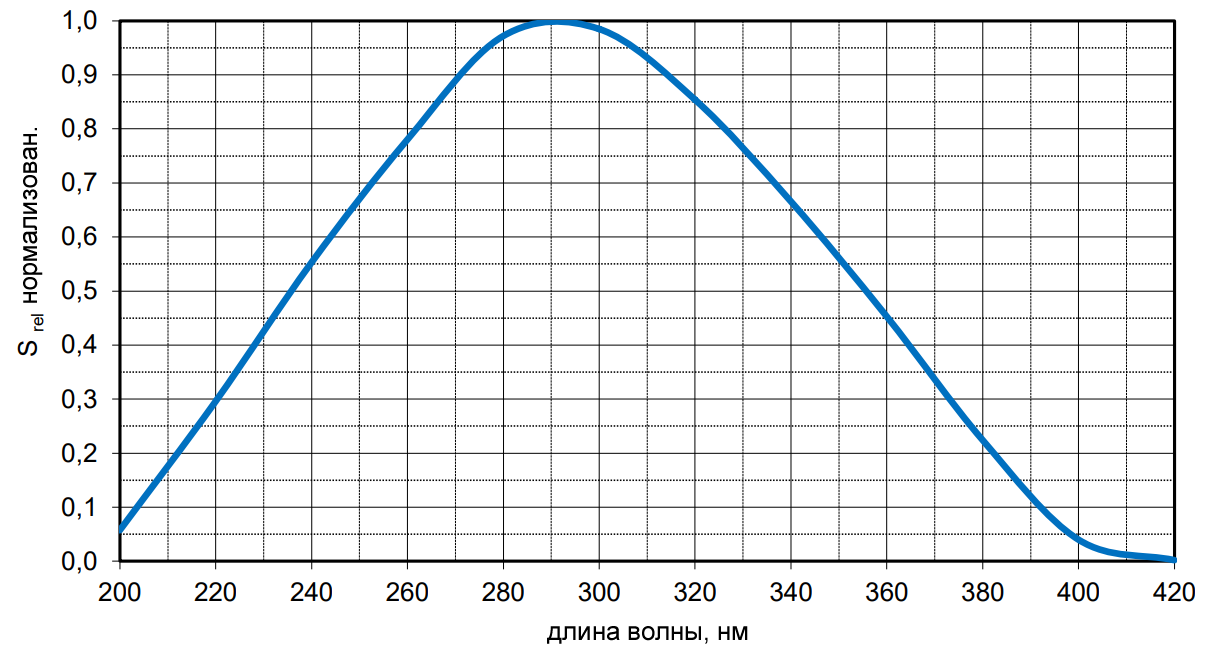 Рисунок 2 – Нормализованный спектральный отклик фотодиода из карбида кремния, производимого Electro Optical Components
Рисунок 2 – Нормализованный спектральный отклик фотодиода из карбида кремния, производимого Electro Optical Components
Этот ограниченный спектральный отклик означает, что SiC-фотодиоды не требуют оптической фильтрации в системах, которые должны предотвращать влияние видимого или инфракрасного света на измерения в ультрафиолетовом диапазоне.
Если вам необходимо только расширить чувствительность до ультрафиолетового излучения, кремниевые ультрафиолетовые фотодиоды – это именно то, что вам нужно. Они сохраняют свою чувствительность в видимом диапазоне; на самом деле их чувствительность к видимому свету намного выше, чем к инфракрасному излучению.
Математическая зависимость между силой падающего света и генерируемым фототоком называется чувствительностью. Пиковая чувствительность SiC-фотодиодов довольно низкая по сравнению с пиковой чувствительностью кремниевых фотодиодов, но пиковая чувствительность кремния не имеет отношения к ультрафиолетовым приложениям, потому что она возникает далеко от длин волн ультрафиолетового излучения. Чувствительность SiC аналогична чувствительности кремния, если мы говорим только про участок спектра 200–400 нм.
Методы глубокой очистки индия и мышьяка.
Для получения монокристаллов арсенида индия с высокими и стабильными электрофизическими параметрами необходимо использовать высокочистые исходные материалы.
Арсенид индия с трудом поддается очистке кристаллизационными методами в следствие высокого давления диссоциации при температуре плавления, высокой химической активности индия и мышьяка при температуре выращивания и близких к единице значений коэффициентов распределения основных примесей в исходных элементах, таких как сера, селен, цинк и др., а также из-за загрязнением кремнием из кварца при высокой температуре.
Методы глубокой очистки индия.
В индии предназначенном для синтеза полупроводниковых соединений, лимитирующими являются следующие примеси: алюминий, медь, магний, кремний, серебро, кальций, серебро и сера.
Применяемые методы очистки индия можно разделить на химические и физические. Методы первой группы — субхлоридный, экстракционный, электролитический и перекристаллизация солей из растворов. Химические методы требуют наличия сверхчистых вспомогательных материалов кислот, щелочей, органических растворителей. Методы второй группы (физические) — термообработка, ректификация, вытягивание из расплава и зонная плавка — включают воздействие на индий каких-либо вспомогательных химических реактивов.
При применении для приготовлении электролита особо чистого натрия электролитическое рафинирование индия позволяет получить индий чистотой 99,9999% (выход по току 90%).
Субхлоридный метод получения индия высокой чистоты позволяет получать индий чистотой 99,9999%.
Для успешного осуществления метода вакуумной термообработки необходимо выполнения следующих условий:
- материал контейнера должен быть достаточно чистым и не взаимодействовать с расплавленном индием;
- термообработка должна проводится в условиях высокого вакуума (10-6 мм рт.ст.) и в остаточной атмосфере, не содержащей углеводородов.
Термообработка индия проводится в интервале температур 500-900ОС. Верхний предел температурного интервала ограничивается взаимодействием расплавленного индия с кварцем и значительным увеличение упругости пара индия.
Вакуумная термообработка позволяет получить индий чистотой 99,9999%.
Зонная плавка электрически рафинированного индия позволяет осуществлять дальнейшую очистку его от примесей.
При вытягивании кристаллов индия по методу Чохральского эффективная очистка происходит при выращивании кристаллов с большими скоростями вращения затравки (60-100 об/мин) и скоростью роста 2см/ч. Чистота индия выращенного по методу Чохральского, выше 99,9999%. Применение только одного способа очистки индия может оказаться недостаточным, и возможно потребуется сочетание различных способов (физических и химических).
Методы получения мышьяка и его соединений высокой степени чистоты.
Общее содержание примесей в мышьяке используемом для синтеза арсенида индия, не должно превышать 1?10-5%, суммарное содержание селена и теллура должно быть < 1?10-6% каждого в отдельности.
Наиболее перспективными технологиями очистки мышьяка являются хлоридная и гидридная с получением промежуточных высоко чистых продуктов треххлористого мышьяка или гидрида мышьяка. Хлоридная схема получения чистого мышьяка включает:
- хлорирование металлического мышьяка хлором или взаимодействие трехокиси мышьяка с соляной кислотой;
- очистку трихлорида мышьяка ректификацией;
- восстановление очищенного трихлорида мышьяка водородом до компактного металлического мышьяка.
Перед ректификацией треххлорида мышьяка проводят сорбционную очистку.
Для получения особо чистых гидрида мышьяка и элементарного мышьяка используется гидридная схема. Гидридная технология мышьяка имеет ряд преимуществ:
- содержание мышьяка в гидриде выше, чем в любом другом соединении;
- разложение гидрида мышьяка происходит при невысоких температурах и отсутствует необходимость в восстановлении;
- гидриды имеют малую реакционную способность по отношению к конструкционным материалам при температурах синтеза и очистки.
Недостатками гидрида мышьяка являются высокая токсичность и взрывоопасность.
Гидридная технология очистки мышьяка состоит из следующих этапов:
- синтез арсенида металла II группы;
- гидролиз арсенида с получением арсина;
- очистка арсина сорбцией;
- вымораживание и ректификация;
- разложение арсина до металлического мышьяка.
Мышьяк, полученный по приведенным схемам, с успехом используется для синтеза арсенида индия. Кроме того, треххлористый мышьяк находит широкое применение для нарашивания эпитаксиальных слоев арсенида индия.
Геохимия и минералогия
Учитывая электронную структуру атома индия, он относится к халькофильным элементам (18 электронов в предпоследнем слое). В настоящее время известно менее 10 индиевых минералов: самородный индий, рокезит CuInS2, индит FeIn2S4, кадмоиндит CdIn2S4, джалиндит In(OH)3, сакуранит (CuZnFe)3InS4 и патрукит (Cu,Fe,Zn)2(Sn,In)S4. В основном индий находится в виде изоморфной примеси в раннем высокожелезистом сфалерите, где его содержание достигает десятых долей процента. В некоторых разновидностях халькопирита и станнина содержание индия составляет сотые-десятые процента, а в касситерите и пирротине — тысячные доли процента. В пирите, арсенопирите, вольфрамите и некоторых других минералах концентрация индия — граммы на тонну. Промышленное значение для получения металла пока имеют сфалерит и другие минералы, содержащие не менее 0,1 % индия. Индий самостоятельных месторождений не образует, а входит в состав руд месторождений других металлов. Наиболее высокое содержание индия установлено в рудах касситеритоносных скарнов и сульфидно-касситеритовых месторождений различных типов. Содержание индия в земной коре (кларк) 0,25 г/т (он в три раза более распространён, чем серебро), в морской воде 0,018 мг/л.
Электрофизические свойства объемного арсенида индия.
Зонная структура арсенида индия.
Зона проводимости. Арсенид индия является прямозонным полупроводником, у которого зона проводимости сферически симметрична и минимум ее находится в центре зоны Бриллюэна. Вблизи минимума кривизна зоны велика, вследствие чего эффективная масса электрона очень мала и равна me»0.026 m0.
Зона проводимости имеет не-параболичную форму, кривизна ее уменьшается с увеличением энергии. Экспериментальные результаты подтверждают непараболичность зоны проводимости. Измерение эффективной массы на поверхности уровня Ферми, приведенное для образцов с различной концентрацией электронов, показало увеличение эффективной массы с ростом n-кол-личеством носителей заряда (рис.1).Рис.1. Зависимость эффективной массы электрона от концентрации электронов.
Валентная зона.
Расчеты зоной структуры валентной зоны показали, что зона тяжелых дырок состоит из двух подзон, сдвинутых относительно точки
=0 в направлении на величину 0.008 а-1б .
В максимумах энергии не более чем на 0.006 эВ превышает энергию, соответствующую центру зоны Бриллюэна. Зона легких дырок вырождена с зоной тяжелых дырок при
=0. Имеется также третья зона, положение которой обусловлено спин-орбитальным взаимодействием. Величина эффективных масс и некоторые характеристики зонной структуры приведены ниже:

Оптические свойства арсенида индия.
Наибольший практический интерес представляет спектральный диапазон в близи края собственного поглощения. Именно в этой области длин волн (3-5 мкм) работают фотоприемники, изготовленные из эпитаксиальных структур арсенида индия.
Поглощение света в толстом полупроводника может быть описано выражением
![]()
где I0 — интенсивность падающего излучения, k — коэффициент отражения, a — коэффициент поглощения, X — координата.
Величина коэффициента отражения в близи края собственного поглощения не превышает 30-40% и может быть оценена из выражения
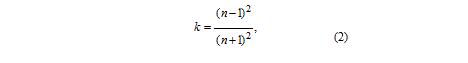
где n — показатель преломления.
- В полупроводниках, как правило, одновременно работает несколько механизмов поглощения света. Основные из них:
- собственное или фундаментальное поглощение;
- эксионное;
- поглощение свободными носителями;
- решетчатое;
- внутризонное.
Полный коэффициент поглощения в случае одновременного участия нескольких механизмов поглощения равен:
. (3)
В указанном диапазоне длин волн 3-5 мкм и обычно используемой области температур 77-300 К работает в основном два механизма: собственное поглощение и поглощение на свободных носителях. В области собственного поглощения прямозонная структура арсенида индия обуславливает резкую зависимость коэффициента поглощения от энергии:
, (4)
где e — заряд электрона, h — постоянная Планка, с — скорость света. В арсениде индия n-типа величина Еg=0.35 эВ при Т=300 К, а показатель степени в выражении для a=0.85 n=1, в материале р-типа Еg=0.36 эВ, а n=0.5.
В легированных образцах за счет малой эффективной массы электронов с увеличением концентрации носителей происходит быстрое заполнение зоны проводимости электронами, в следствии чего уровень Ферми находится выше дна зоны проводимости на величину энергии DEn. В этом случае коэффициент поглощения описывается выражением (5)
т.е. происходит сдвиг края поглощения в сторону больших энергий.
Поглощение на свободных носителях в области длин волн, превышающих 3 мкм, хотя слабее, чем собственное, тем не менее может играть значительную роль в сильно легированных образцах. В этом случае a описывается выражением (6)
где n — показатель преломления, s — проводимость, l — длина волны,
Оценки показывают, что при l=3 мкм и n=1018 см-3 в пластине арсенида индия толщиной 400 мкм поглотится около 80% светового потока.
Подвижность в арсениде индия.
Подвижность носителей заряда в кристаллах арсенида индия ограничивается несколькими механизмами рассеивания:
- рассеянием на оптических и акустических фононах;
- на ионных примесях;
- на нейтральных примесях:
- на дефектах кристаллической решетки (дислокациях):
- на носителях заряда.
В приближении времени релаксации t подвижность вычисляется по формуле (7)
где t — вычисляется для каждого механизма рассеивания отдельно.
В монокристаллических объемных образцах арсенида индия достигнуты следующие значения подвижности:
n-тип, m=30000 см2/Вс(300К),
р-тип, m=450 см2/Вс(300К).
Сростом концентрацией примесей подвижность падает.
Как составить уравнение реакции
Одно из самых распространенных заданий на экзаменах и в контрольных работах – составить уравнение на реакцию HCl, в данном случае – соляной, с другими веществами или соединениями.
Чтобы не запутаться в решении, предлагаем несколько советов и шпаргалок для легкого запоминания:
- Запомните буквенное обозначение данного вещества – соляная кислота в химии обозначается как HCl: если вещество разбавленное, это указывается в скобках рядом.
- Как уже было сказано выше, вещество способно реагировать с активными металлами, стоящими до водорода в электрохимическом ряду; кроме того, она реагирует на основания, оксиды, гидроксиды и карбонаты.
- Химические основания обозначаются как OH, оксиды – O, гидроксиды – OH2, карбонаты – CO3.
- Уравнение реакции всегда будет иметь знак +, потому как в процессе взаимодействия происходит соединение нескольких компонентов.
- HCl может идти первым или вторым слагаемым, после прибавления металла, вещества идет знак =, после этого описывается реакция, где указаны продукты распада.
- Например, при реакции кислоты серы с сульфатом магния получается такое уравнение: Mg+H2SO4 = MgSO4+H2.
- Соляная кислота и гидроксид бария дают такое уравнение: 2HCl + Ba(OH)2 = BaCl2 + 2H2O.
- При реакции соединения водорода, хлора и мела образуется хлорид кальция: СаСО3 + 2HCl = CaCl2 + СО2 + Н2О.
- Раствор карбоната натрия с кислотой выглядит так: HCl+Na2CO3=2NaCl+H2O+CO2.
Составить уравнение несложно, важно изначально правильно обозначить буквенные символы каждого элемента или вещества. Важно! Необходимо правильно определить коэффициенты атомов в уравнении – их количество до знака = должно быть таким же, как и после знака =.
Важно! Необходимо правильно определить коэффициенты атомов в уравнении – их количество до знака = должно быть таким же, как и после знака =.
Для правильного уравновешивания формулы пользуются правилами школьного курса химии, основанными на математическом принципе расстановки коэффициентов.
Инфракрасные детекторы
Антимонид индия (InSb)
Когда я думаю о фотодиодах, первое, что приходит на ум, – это InSb. Он гораздо менее распространен, чем кремний, но он запечатлелся в моем инженерном сознании, потому что один из самых важных корпоративных проектов, над которыми я когда-либо работал, был основан на массиве фотодиодов из InSb.
InSb чувствителен к коротковолновому и средневолновому инфракрасному излучению и предлагает отличную производительность для приложений, которые вместо видимого света должны обнаруживать тепловые сигнатуры. Однако чтобы максимально использовать InSb, вам нужно приложить дополнительные усилия, а именно охладить фотодиод до криогенных температур. Это делается с помощью сосудов Дьюара, в которых находится диод и жидкий азот. Вы заполняете сосуд Дьюара жидким азотом, и тогда ваш детектор из InSb будет готов к обеспечению максимальной чувствительности.
Арсенид галлия-индия (InGaAs) и германий (Ge)
InGaAs широко используется в качестве материала для быстродействующих и высокочувствительных детекторов инфракрасного излучения. В отличие от InSb, он обычно используется при комнатной температуре и имеет небольшое увеличение чувствительности на более коротких длинах волн: InSb работает примерно до 1 мкм, тогда как диапазон InGaAs снижен примерно до 0,7 мкм.
Германий похож на InGaAs в отношении спектрального отклика и работает при комнатной температуре. Но InGaAs может достичь значительно более высокого отношения сигнал/шум.
Теллурид кадмия-ртути (HgCdTe)
Теллурид кадмия-ртути играет важную роль в детекторах для длинноволновых инфракрасных приложений. Спектральный отклик InGaAs и InSb сужен до 2–3 мкм и 5–6 мкм соответственно, тогда как диапазон HgCdTe простирается до 16 мкм. Длинноволновый инфракрасный диапазон (LWIR, long-wavelength IR) используется для пассивного теплового обнаружения и визуализации.
Как и детекторы из InSb, детекторы из HgCdTe охлаждаются до криогенных температур. Это серьезное неудобство, и многие устройства для получения изображений LWIR используют неохлаждаемые микроболометры; микроболометры реагируют непосредственно на тепловую энергию, в отличие от фотодиодов, которые реагируют на падающие фотоны электромагнитного излучения. Микроболометры дешевле, меньше по размеру и более энергоэффективны; но детекторы из HgCdTe создают изображения более высокого качества.
Биологическая роль
Индий не имеет ярко выраженной метаболической роли в организме. Соединения индия не всасываются в желудочно-кишечном тракте, умеренно всасываются при вдыхании. Индий может временно накапливаться в мышцах, коже и костях человека, его период полувыведения около двух недель. Растворимые соединения индия с валентностью III могут быть токсичными для почек при введении путем инъекции. Длительное вдыхание паров или мелкодисперсной пыли индия, его оксида или гидроксида может вызывать болезнь легких, получившую название Indium lung.
Предельно допустимая концентрация индия в воздухе рабочей зоны 0,1 мг/м3 (Национальный институт охраны труда, США). Однако после появления сведений о заболеваниях легких правила стали ужесточать. Так, японский национальный институт безопасности и гигиены труда установил ПДК на уровне 0.0003 мг/м3.
Химические свойства
- Электроотрицательность — 1,78.
- Устойчив и не тускнеет в сухом воздухе при комнатной температуре, но выше 800 °C горит фиолетово-синим пламенем с образованием оксида.
- Растворяется в серной и соляной кислотах, быстрее — в азотной и хлорной, с плавиковой кислотой медленно реагирует при нагревании, органические кислоты (муравьиная, уксусная, щавелевая, лимонная) постепенно растворяют индий.
- С растворами щелочей, даже кипящими, заметно не реагирует.
- Реагирует с хлором и бромом.
- При нагревании реагирует с йодом, серой (выше 620 °C), селеном, теллуром, диоксидом серы (выше 600 °C), парами фосфора.
- Степень окисления от +1 до +3, наиболее устойчивы 3-валентные соединения.
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.

В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.

При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
Реакции с неметаллами
Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2, если разбавленная — до NO.

В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты.
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.

Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
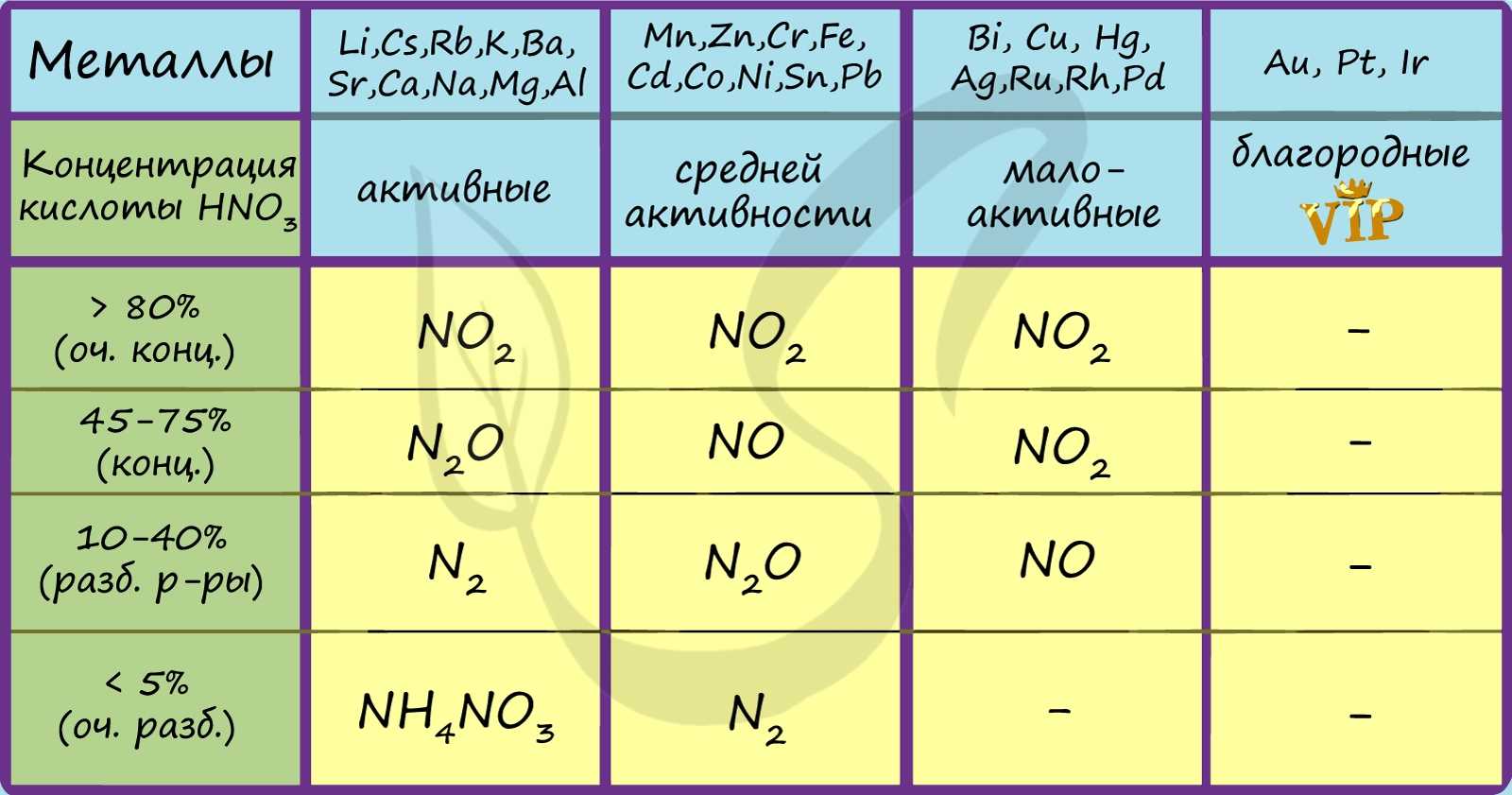
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Соли азотной кислоты — нитраты NO3 —
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.

Нитрат аммония получают реакция аммиака с азотной кислотой.
Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная кислота — до +2
- Реакции с металлами, основаниями и кислотами
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).

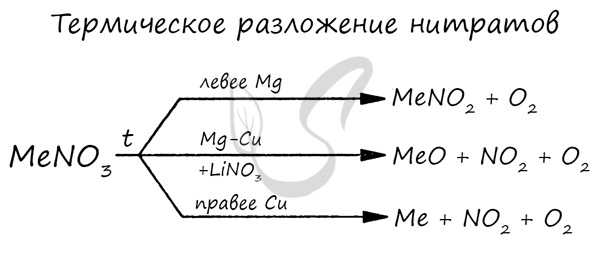
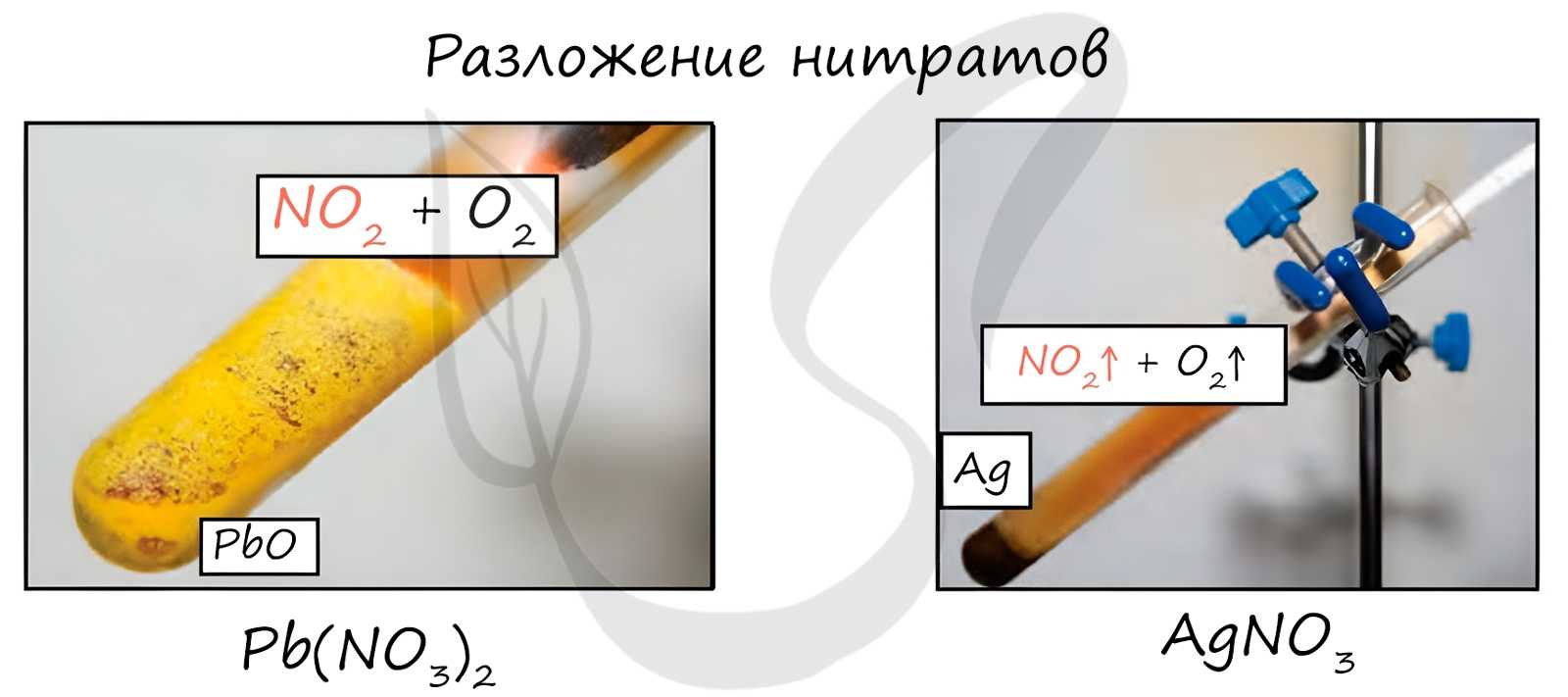
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.
Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Какие вещества вступают в реакцию с соляной кислотой
На вступительных экзаменах по химии часто можно встретить задание на определение веществ, которые способны реагировать на соляную кислоту.
Кроме того, задание «составьте уравнение» нередко вызывает страх в глазах выпускников.
Чтобы не путаться с химическими задачами, рекомендуется подробнее изучить информацию о взаимодействии с данным соединением.
Все существующие вещества можно поделить на металлы, вытесняющие водород из соединения, не вытесняющие водород, а также активные и неактивные металлы.
В реакцию с соляной кислотой вступают такие вещества:
-
Химические основания. Соляная кислота способна нейтрализовать основания. Как известно, они состоят из атома металла, на который и воздействует кислота.
К ним относят гидроксид натрия, бария, алюминия. Реакция нейтрализации дает образования соли и воды. -
Металлы. Если обратиться к электрохимическому ряду, можно увидеть, что соляная кислота реагирует со всеми элементами, стоящими до водорода в этом ряду.
Сюда относят натрий, магний, алюминий, литий, барий, кальций, цинк, железо и другие элементы. При взаимодействии они образуют хлориды и выделяют газообразный водород. - Основные и атмосферные оксиды. Во время реакции происходит образование растворимых солей и воды. HCl взаимодействует с оксидом алюминия, меди, цинка, натрия.
-
Карбонаты. При взаимодействии с карбонатами кальция получится следующее уравнение: CaCO₃ + 2HCl→ CaCl₂ + CO₂↑ + H₂O.
Из него следует, что выделяется углекислый газ, а также образуется вода и угольная кислота. - Сильные окислители. Если вещество взаимодействует с перманганатом калия или диоксидом марганца, на выходе получается выделение газообразного хлора.
- Аммиак. Такое взаимодействие ознаменовано выделением сильного дыма, поэтому в момент проведения опытов рекомендуется открыть все окна. Тогда выделяется хлорид аммония.
Кроме перечисленных веществ и соединений, HCl также способна реагировать на нитрат серебра – при таком взаимодействии образуется осадок белого цвета творожистого типа.
Физические свойства серной кислоты
При
обычных условиях серная кислота –
тяжёлая маслянистая жидкость без цвета
и запаха. В технике серной кислотой
называют её смеси как с водой, так и с
серным ангидридом. Если молярное
отношение SO 3:
Н 2 О
меньше 1, то это водный раствор серной
кислоты, если больше 1, – раствор SO 3 в
серной кислоте.
100 %-ная
H 2 SO 4 кристаллизуется
при 10,45 °С; Т
кип =
296,2 °С; плотность 1,98 г/см 3 .
H 2 SO 4 смешивается
с Н 2 О
и SO 3 в
любых соотношениях с образованием
гидратов, теплота гидратации настолько
велика, что смесь может вскипать,
разбрызгиваться и вызывать ожоги.
Поэтому необходимо добавлять кислоту
к воде, а не наоборот, поскольку при
добавлении воды к кислоте более легкая
вода окажется на поверхности кислоты,
где и сосредоточится вся выделяющаяся
теплота.
При
нагревании и кипении водных растворов
серной кислоты, содержащих до 70 %
H 2 SO 4 ,
в паровую фазу выделяются только пары
воды. Над более концентрированными
растворами появляются и пары серной
кислоты.
По
структурным особенностям и аномалиям
жидкая серная кислота похожа на воду.
Здесь та же система водородных связей,
почти такой же пространственный каркас.
Применение
- Широко применяется в производстве жидкокристаллических экранов для нанесения прозрачных плёночных электродов из оксида индия-олова.
- Используется в микроэлектронике как акцепторная примесь к германию и кремнию. Ранее, когда широко применялась сплавная технология производства первых полупроводниковых приборов, характерным решением было сплавление индия с германием для получения pn-перехода, например в диодах серий ДГ-Ц1, Д7 и так далее до сотни мг индия.
- Компонент ряда легкоплавких припоев и сплавов (так, жидкий при комнатной температуре галинстан содержит 21,5 % индия). Обладает высокой адгезией ко многим материалам, позволяя спаивать, например, металл со стеклом. В сплаве с оловом применяется как легкоплавкий припой с высокой теплопроводностью для термоинтерфейсов принудительно охлаждаемых электронных компонентов.
- Иногда применяется (чистый или в сплаве с серебром) для покрытия зеркал, в частности, автомобильных фар, при этом отражающая способность зеркал не хуже, чем у серебряных, а стойкость к воздействию атмосферы (особенно сероводорода) — выше. В покрытии астрономических зеркал используется постоянство коэффициента отражения индия в видимой части спектра.
- Материал для фотоэлементов.
- Соединения используются как люминофоры.
- Покрытие юбок алюминиевых поршней дизельных двигателей для снижения износа.
- Арсенид индия применяется как высокотемпературный термоэлектрический материал с очень высокой эффективностью, для увеличения эффективности обычно легируется 10 % фосфида индия.
- Изотопы индия 111In и 113mIn используются в качестве радиофармацевтических препаратов.
- Точка плавления индия (429,7485 К или 156,5985 °C) — одна из определяющих точек международной температурной шкалы ITS-90.
- Индий входит в состав «голубого золота».
- Электрохимическая система индий-оксид ртути служит для создания чрезвычайно стабильных во времени источников тока (аккумуляторов) высокой удельной энергоёмкости для специальных целей.
- Ортофосфат индия используется в качестве добавки к зубным цементам.
- В технике высокого вакуума индий используется в качестве уплотнителя (прокладки, покрытия); в частности, при герметизации космических аппаратов и мощных ускорителей элементарных частиц.
- Индий имеет высокое сечение захвата тепловых нейтронов и может быть использован для управления атомным реактором, хотя более удобно применение его соединений в комбинации с другими элементами, хорошо захватывающими нейтроны. Так, оксид индия находит применение в атомной технике для изготовления стекла, применяемого для поглощения тепловых нейтронов. Наиболее широко распространённый состав такого стекла — оксид бора (33 %), оксид кадмия (55 %), оксид индия (12 %).
- Изотоп индия 115In предложен для детектирования низкоэнергетических электронных нейтрино : 115In + νe → 115Sn+e−+2γ
Получение
Динамика планетарной добычи индия, по данным USGS
Получают из отходов и промежуточных продуктов производства цинка и, в меньшей степени, свинца и олова. Это сырьё содержит от 0,001 % до 0,1 % индия. Из исходного сырья производят концентрат индия, из концентрата — черновой металл, который затем рафинируют. Исходное сырьё обрабатывают серной кислотой и переводят индий в раствор, из которого гидролитическим осаждением выделяют концентрат. Из концентрата черновой металл извлекают цементацией на цинке и алюминии. Для рафинирования используются различные методы, например, зонная плавка.
Основным производителем индия является Китай (390 тонн в 2012 году), также производится Канадой, Японией и Южной Кореей (примерно по 70 тонн).
В последние годы мировое потребление индия быстро растёт и в 2005 достигло 850 тонн.
Количество используемого индия сильно зависит от мирового производства ЖК-экранов. В 2007 году в мире было добыто 475 тонн и ещё 650 тонн было получено путём переработки. На производство ЖК экранов для компьютерных дисплеев и телевизоров уходило 50—70 % доступного индия.
Стоимость индия в 2002 году составила около 100$ за кг, но рост потребности в металле привёл к повышению и колебаниям цен. В 2006—2009 годах они колебались в пределах 400—900 долларов за кг.
По современным оценкам, запасы индия будут исчерпаны в ближайшие 20 лет, если не будет повышена степень вторичного использования металла.
Признак взаимодействия с цинком, железом и другими металлами
Если курс школьной химии был успешно забыт, можно вспомнить о том, какие бывают признаки взаимодействия металлов, вступающих в реакцию с соляной кислотой.
Чтобы экспериментальные опыты не вызвали несчастного случая, рекомендуется заранее открыть все окна, вооружиться защитной одеждой, чтобы кожа рук была закрыта.
Также рекомендуется использовать перчатки и повязку на лицо.
Обратите внимание! Ниже будет рассказано о том, какие признаки говорят о вступлении в реакцию элементов с соединением.
Чтобы не проводить наглядные опыты, можно воспользоваться теоретической информацией.
Рассмотрим, что происходит, если добавить немного кислоты на определенный вид металла:
| Металл | Признак взаимодействия |
| Цинк | Если опустить этот металл серебристого цвета в пробирку с указанным веществом, можно постепенно наблюдать выделение небольшого количества пузырьков и водорода. В результате возникает хлорид цинка ZnCl₂ |
| Железо | Во время такого взаимодействия образуется хлористое железо. Реакция происходит медленно, однако, если пробирку подогреть, то процесс пойдет быстрее |
| Литий | При реакции образуется хлорид лития 2LiCl, выделяется водород. На поверхности этого металла, относящегося к щелочной группе, можно увидеть маленькие пузыри |
| Кремний | В результате такого соединения возникает сложный компонент под названием хлорсилан. Также выделяется газообразный водород. Такая реакция происходит при условии нагревания до 350 градусов, а в качестве катализатора выступает медь |
| Магний | При таком взаимодействии наблюдает выделение теплоты, металл начинает плавиться |






























