Виды воды[]
Вода на Земле может существовать в трёх основных состояниях — жидком, газообразном и твёрдом и приобретать различные формы, которые могут одновременно соседствовать друг с другом: водяной пар и облака в небе, морская вода и айсберги, ледники и реки на поверхности земли, водоносные слои в земле. Вода способна растворять в себе множество органических и неорганических веществ
Из-за важности воды, «как источника жизни», её нередко подразделяют на типы по различным принципам.
По особенностям происхождения, состава или применения, выделяют, в числе прочего:
Мягкая вода и жёсткая вода — по содержанию катионов кальция и магния
- По изотопам водорода в молекуле:
- Лёгкая вода (по составу почти соответствует обычной)
- Тяжёлая вода (дейтериевая)
- Сверхтяжёлая вода (тритиевая)
- Пресная вода
- Дождевая вода
- Морская вода
- Подземные воды
- Минеральная вода
- Солоноватая вода (en:Brackish water)
- Питьевая вода, Водопроводная вода
- Дистиллированная вода и деионизированная вода
- Сточные воды
- Ливневая вода или поверхностные воды
- Апирогенная вода
- Мёртвая вода и Живая вода — виды воды из сказок (со сказочными свойствами)
- Лёд-девять (вымышленный материал)
- Святая вода — особый вид воды согласно религиозным учениям
- Поливода
- Структурированная вода — термин, применяемый в различных неакадемических теориях.
- Талая вода
Химические названия воды
С формальной точки зрения вода имеет несколько различных корректных химических названий:
- Оксид водорода: бинарное соединение водорода с атомом кислорода в степени окисления −2
- Монооксид дигидрогена
- Гидроксид водорода: соединение гидроксильной группы OH- и катиона (H+)
- Гидроксильная кислота: воду можно рассматривать как соединение катиона H+, который может быть замещён металлом, и «кислотного остатка» OH-
- Оксидан
- Дигидромонооксид
Краткая теория
Основу термодинамики составляют два
начала. Первое начало устанавливает
количественные соотношения, имеющие
место при превращениях энергии из одних
видов в другие. Оно утверждает: количество
теплоты 5,
5,
переданное системе, увеличивает ее
внутреннюю энергию на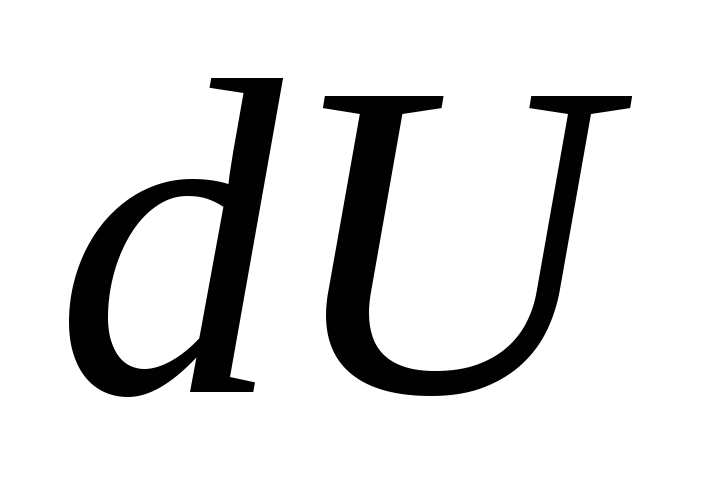 и превращается в работу
и превращается в работу ,
,
совершаемую системой против внешних
сил:
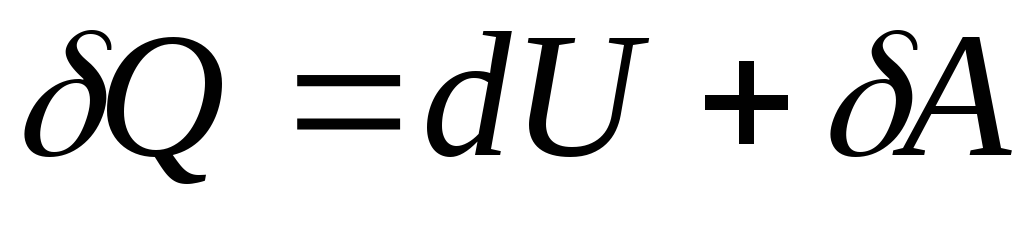
Второе
начало термодинамики определяет условия,
при которых возможны превращения
энергии, т.е. определяет возможные
направления процессов, происходящих в
системе.
Величины,
характеризующие состояния системы,
называются параметрами состояния.
Состояние системы, при котором все
параметры имеют значения, остающиеся
неизменными сколь угодно долго, называется
равновесным. Равновесный процесс может
быть проведен в обратном направлении
(обратный процесс) через те же промежуточные
состояния, что и прямой.
Функция S, дифференциал
которой
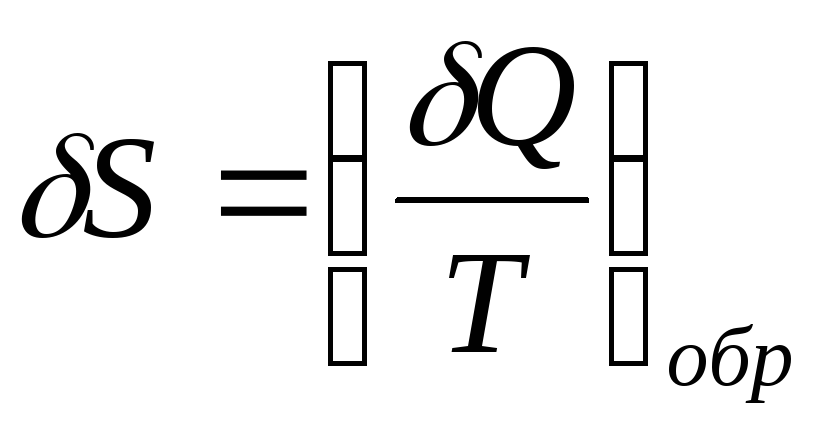
называется энтропией
системы. Здесь
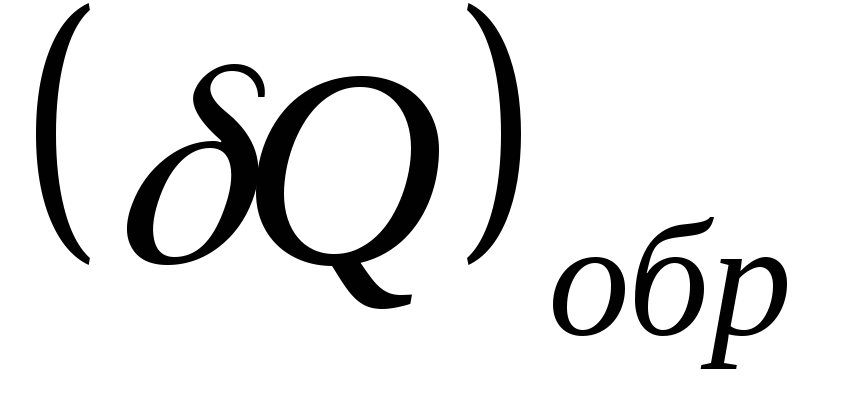 Т
Т
Если
количество теплоты  сообщается системе в ходе необратимого
сообщается системе в ходе необратимого
процесса, то энтропия возрастает как
вследствие сообщения тепла, так и
вследствие необратимости процесса.
Поэтому
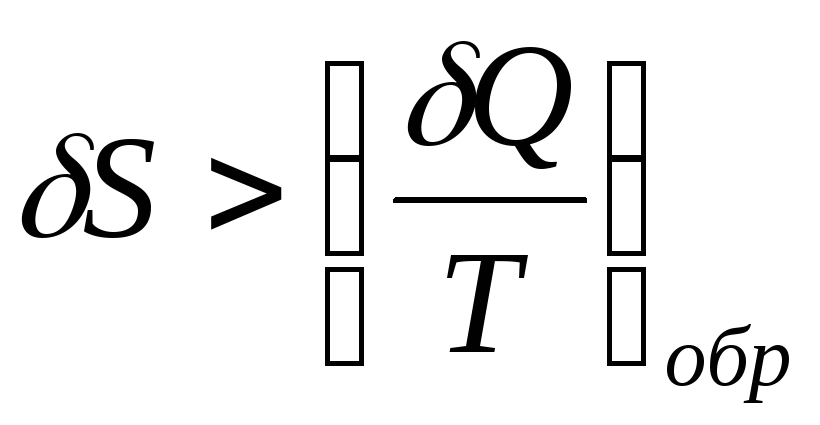
Формулы
(10.2) и (10.3) можно объединить
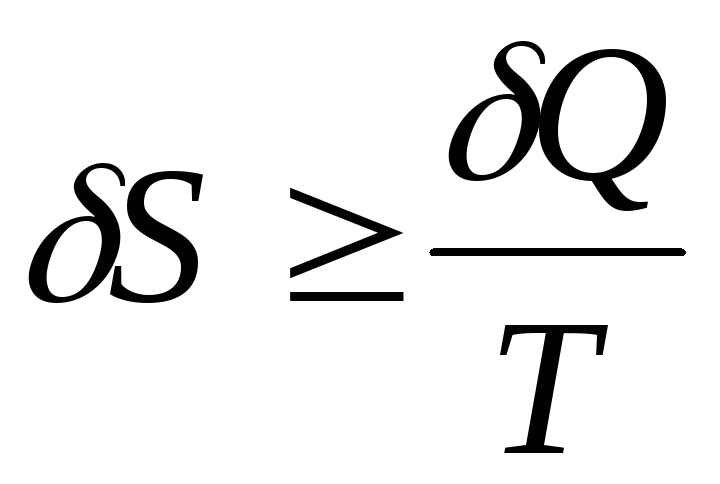
Знак равенства относится
к обратимым, знак неравенства – к
необратимым процессам.
Состояние
макроскопического тела или макросостояние
может быть осуществлено различными
способами, каждому из которых соответствует
некоторое микросостояние тела. Число
различных микросостояний, соответствующих
данному макросостоянию, называется
статистическим весом или термодинамической
вероятностью макросостояния Ω. Энтропия
системы пропорциональна Ω:
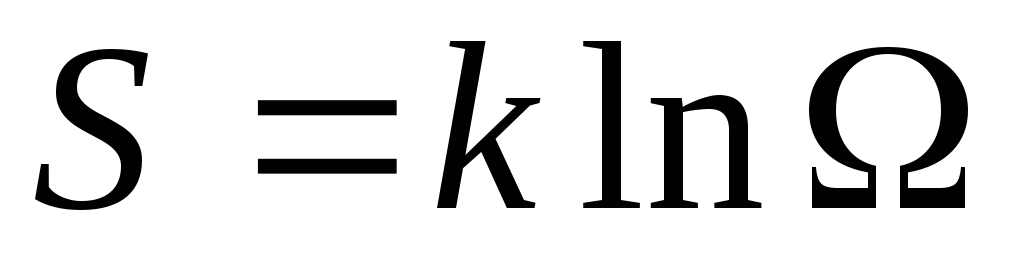
Энтропия
изолированной системы при протекании
необратимого процесса возрастает,
стремясь к максимуму. Действительно,
изолированная система переходит из
менее вероятных в более вероятные
состояния, что сопровождается ростом
Ω и S. Это максимальное
значение достигается системой, когда
она переходит в состояние термодинамического
равновесия:

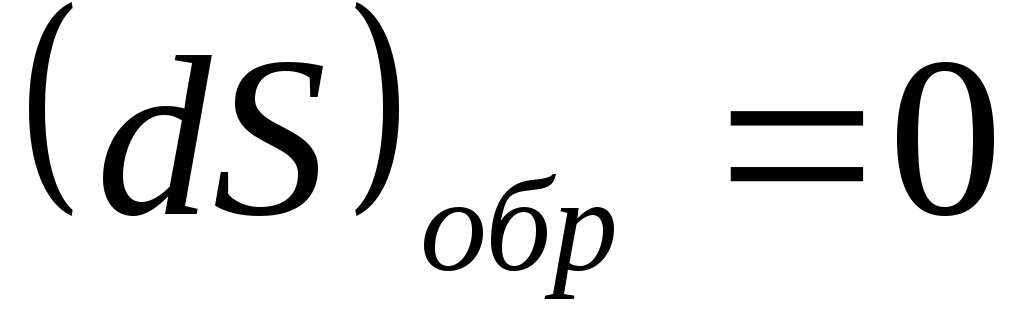
Энтропия изолированной
системы не может убывать:
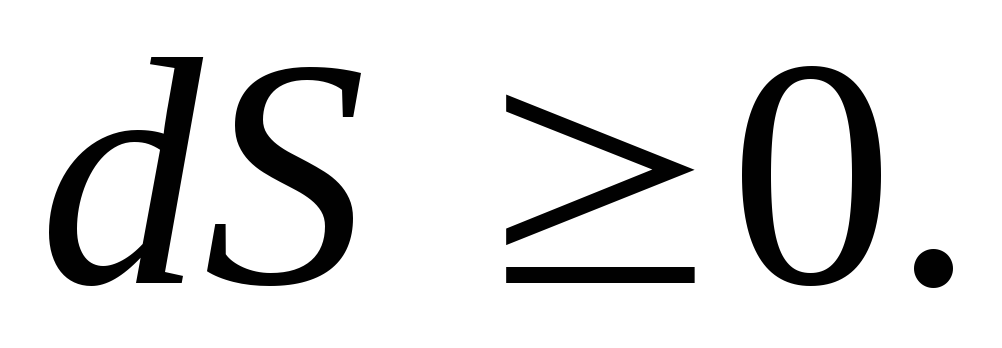
Это утверждение одна
из формулировок второго начала
термодинамики.
Изменение
энтропии в обратимом процессе равно
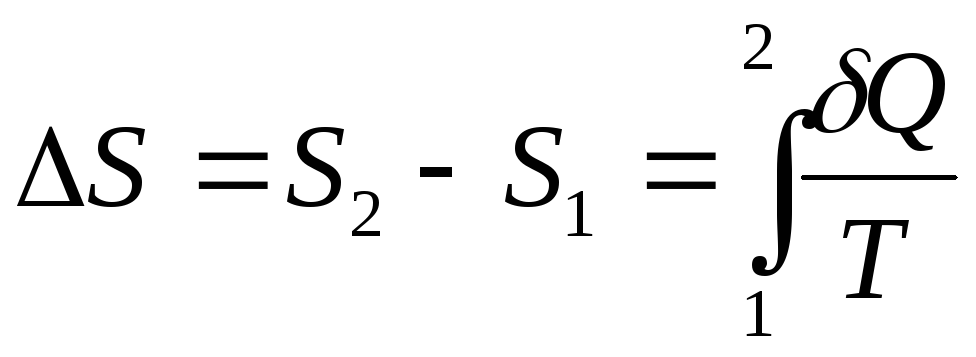
По знаку
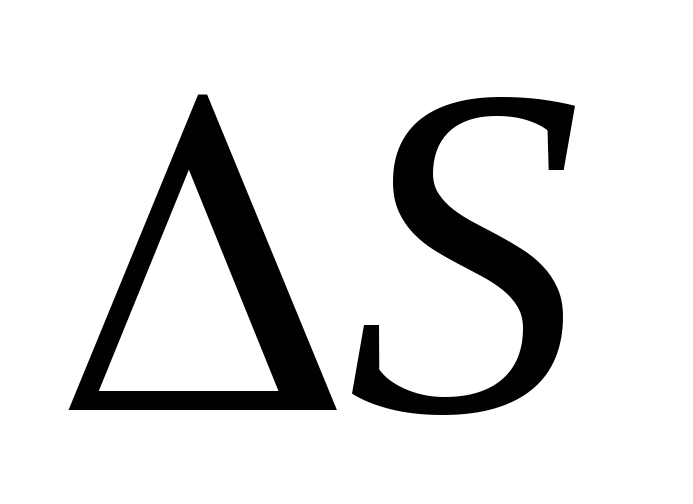
Полезные советы
Всегда помните, что:
- процесс нагревания металла проходит быстрее, чем у воды, так как он обладает CP в 2,5 раза меньше;
- по возможности преобразуйте полученные результаты в более высокий порядок, если позволяют условия;
- в целях проверки результатов можно воспользоваться интернетом и посмотреть с для расчётного вещества;
- при равных экспериментальных условиях более значительные температурные изменения будут наблюдаться у материалов с низкой удельной теплоёмкостью.
- https://LivePosts.ru/articles/education-articles/fizika/formula-dlya-raschyota-udelnoj-teployomkosti-veshhestva
- https://formulki.ru/molekulyarka/kolichestvo-teploty-i-udelnaya-teploemkost
- https://www.syl.ru/article/222076/mod_udelnaya-teploemkost-dlya-chego-ona-nujna-i-v-chem-ee-smyisl
- http://al-vo.ru/teplotekhnika/raschet-teplovoy-moshchnosti.html
- https://skysmart.ru/articles/physics/udelnaya-teploemkost-veshestva
- https://www.webmath.ru/poleznoe/formules_21_24_kolichestvo_teploty.php
- https://obrazovaka.ru/fizika/udelnaya-teploemkost-formula.html
Единица измерения количества теплоты: все, что вам нужно знать
Предположим, нам нужно повысить на 50 градусов Цельсия температуру воды в каждой кастрюльке. Примечание: После нагревания воды на 50 градусов, конечная температура воды в каждой кастрюльке будет равна 70 градусам. Чтобы нагреть на 50 градусов 1 килограмм воды, потребуется время. Однако, чтобы нагреть на этой же конфорке 2 килограмма воды на 50 градусов, потребуется больше времени. Значит, количество теплоты, полученное водой, зависит от массы вещества, которое мы хотим нагреть. От разницы температур Теперь возьмем две кастрюльки, и нальем в них по 1 кг воды. Одну кастрюльку будем нагревать дольше другой. Поэтому, температура воды будет выше в той кастрюльке, которую дольше нагревали. Так как температура повысилась больше в кастрюльке, которую дольше нагревали, то физики скажут, что воде в этой кастрюльке передали большее количество теплоты. Значит, количество теплоты зависит от разницы т.
От вида вещества Теперь будем нагревать 1 килограмм воды и 1 килограмм подсолнечного масла. Измерим через 5 минут нагревания температуру воды и температуру масла. Оказывается, за 5 минут масло нагреется до более высокой температуры. При этом и масло, и вода, получили одинаковое количество теплоты. Значит, количество теплоты зависит от того, из какого вещества состоит тело. Количество теплоты зависит от массы и вида вещества, а, так же, от разницы температур Какие величины называют удельными Физики часто применяют удельные величины, так как они достаточно удобны для вычислений.
Это такие точки в системе двух массивных небесных тел, в которых воздействие их на третье тело пренебрежимой массы оказывается одинаковым… Ответ на опрос: Что такое «экзопланета»? Экзопланета — это просто планета у другой звезды… Ответ на опрос: Как обозначаются звезды на звездных картах? Для обозначения звезд используются буквы греческого алфавита, причем,…
Именно эту тепловую энергию вода получила во время нагревания. Потому, что выполняется закон сохранения тепловой энергии. Теплота, как и любая энергия, измеряется в системе СИ в Джоулях, в честь английского физика Джеймса Джоуля. Что такое количество теплоты Примечание: Количество теплоты, так же, измеряют в Калориях. Калория — это тепловая энергия, затраченная на нагревание 1 грамма воды на 1 градус Цельсия. От массы вещества Нальем в одну кастрюльку 1 кг воды, а в другую, точно такую же кастрюльку — 2 килограмма воды. Будем нагревать эти кастрюльки по очереди на газовой плите, не меняя интенсивность огня конфорки. Предположим, нам нужно повысить на 50 градусов Цельсия температуру воды в каждой кастрюльке. Примечание: После нагревания воды на 50 градусов, конечная температура воды в каждой кастрюльке будет равна 70 градусам. Чтобы нагреть на 50 градусов 1 килограмм воды, потребуется время. Однако, чтобы нагреть на этой же конфорке 2 килограмма воды на 50 градусов, потребуется больше времени. Значит, количество теплоты, полученное водой, зависит от массы вещества, которое мы хотим нагреть. От разницы температур Теперь возьмем две кастрюльки, и нальем в них по 1 кг воды. Одну кастрюльку будем нагревать дольше другой. Поэтому, температура воды будет выше в той кастрюльке, которую дольше нагревали. Так как температура повысилась больше в кастрюльке, которую дольше нагревали, то физики скажут, что воде в этой кастрюльке передали большее количество теплоты.
Значит, количество теплоты зависит от разницы т. От вида вещества Теперь будем нагревать 1 килограмм воды и 1 килограмм подсолнечного масла. Измерим через 5 минут нагревания температуру воды и температуру масла. Оказывается, за 5 минут масло нагреется до более высокой температуры. При этом и масло, и вода, получили одинаковое количество теплоты. Значит, количество теплоты зависит от того, из какого вещества состоит тело. Количество теплоты зависит от массы и вида вещества, а, так же, от разницы температур Какие величины называют удельными Физики часто применяют удельные величины, так как они достаточно удобны для вычислений. Удельная величина — величина, приходящаяся на единицу массы, длины, площади, или объема. Удельная величина — это величина, приходящаяся на единицу чего-либо например, массы, длины и т. В обычной жизни мы, так же, пользуемся удельными величинами. К примеру, цена товара — это удельная величина, так как она приходится на единицу товара. Зная количество товара, легко посчитать общую цену покупки. Например, булочка стоит 20 рублей. Нужно купить 3 булочки. Общую сумму денег найдем, перемножив цену одной булочки удельную величину на количество штук. Известно, что при горении топлива выделяется энергия.
Накопительные водонагреватели (бойлеры)
Без физико-математических формул бытовой расчёт описывается следующим образом: за 1 час 1 кВт нагревает 860 литров на 1 К. Для более точного определения времени нагревания, мощностных характеристик, объёма используется универсальная формула, из которой потом выводятся остальные результаты:
Эта формула состоит из нескольких и отражает целый ряд параметров, учитывая при этом фактор теплопотерь. (При малых мощностных характеристиках и большом объёме этот фактор становится более существенным, однако в бытовых нагревателях этим учётным значением чаще пренебрегают):
Nfull – мощностные характеристики нагревательного элемента,
Qc – теплопотери водонагревательной ёмкости.
- c= Q/m*(tк-tн)
- С – удельная теплоёмкость,
- Q – количество теплоты,
- m – масса в килограммах (либо объём в литрах),
- tк и tн (в °С) – конечная и начальная температуры.
- N=Q/t
- N – мощностные характеристики нагрева.
- t — время нагревания в секундах.
- N = Nfull — (1000/24)*Qc
Упрощенные формулы с постоянным коэффициентом:
- Расчёт мощности ТЭНа для нагрева воды нужной температуры: W= 0,00117*V*(tк-tн)/T
- Определение времени, необходимого для нагревания воды в водонагревателе: T= 0,00117*V*(tк-tн)/W
Составляющие формул:
- W (в кВТ) – мощностная характеристика ТЭНов (нагревательного элемента),
- Т (в часах) – время нагрева воды,
- V (в литрах) – объем бака,
- tк и tн (в °С) – конечная и начальная температуры (конечная – обычно 60°C).
Часто объём приравнивают к массе (m). Тогда определение мощности ТЭНа будет производиться по формуле: W= 0,00117*m*(tк-tн)/T. Формулы считаются упрощёнными, ещё и потому что в них не учитывается:
- фактическая мощность электросети,
- температура окружающей среды,
- конструктивные особенности и потенциальные теплопотери бака,
- рекомендации некоторых производителей, относительно tн (порядка 5-8 °С летом и 15-18 °С – зимой).
При покупке устройства надо принимать во вниание, что относительно низкие мощностные характеристики накопительных водонагревателей по сравнению с проточными ещё не гарантируют финансовую экономию. Накопительные меньше «забирают», но из-за того, что работают дольше, больше и расходуют. Хотите увидеть классные видеоролики, в которых женщины готовы отдаваться мужикам долго и в разных позах, тогда бесплатное порно https://www.faphub.tv/ можно найти, перейдя на данный сайт. Вы не пожалеете, что попали сюда, так как видео тут на любой вкус. Для финансовой экономии более надёжной стратегией будет общее снижение водопотребления за счёт установки различного вида экономителей (https://water-save.com/) и строгий учёт водорасхода.
Температурные единицы
Для измерения температуры используются различные единицы измерения. Некоторые наиболее распространенные единицы измерения температуры включают градус Цельсия (°C), градус Фаренгейта (°F) и кельвин (K).
Градус Цельсия — это наиболее распространенная шкала температуры. На этой шкале 0 °C соответствует точке замерзания воды, а 100 °C — точке кипения воды при нормальных атмосферных условиях.
Градус Фаренгейта — это еще одна шкала температуры, которая часто используется в Северной Америке и некоторых других странах. На этой шкале 32 °F соответствует точке замерзания воды, а 212 °F — точке кипения воды при нормальных атмосферных условиях.
Кельвин — это абсолютная шкала температуры, в которой нулевое значение соответствует абсолютному нулю (-273,15 °C). Кельвин используется в научных и технических расчетах, где необходима абсолютная шкала температуры.
Литература[]
Лосев К. С. Вода. — Л.: Гидрометеоиздат, 1989. — 272 с. (см. ISBN )
- Гидробионты в самоочищении вод и биогенной миграции элементов. — М.: МАКС-Пресс. 2008. 200 с. Предисловие члена-корр. РАН В. В. Малахова. (Серия: Наука. Образование. Инновации. Выпуск 9). ISBN 978-5-317-02625-7.
- О некоторых вопросах поддержания качества воды и её самоочищения // Водные ресурсы. 2005. т. 32. № 3. С. 337—347.
- Андреев В. Г. Влияние протонного обменного взаимодействия на строение молекулы воды и прочность водородной связи. Материалы V Международной конференции «Актуальные проблемы науки в России». — Кузнецк 2008, т.3 С. 58-62.
Примеры расчетов количества теплоты
В качестве итога – несколько примеров на расчет количества теплоты в различных ситуациях.
Пример 1 – расчет количества теплоты для нагревания тела
Вычислить величину Q, потребную для нагревания медной пластины весом 2 кг от 25 до 200 градусов.
Для этого надо воспользоваться формулой
Удельная теплоемкость меди берется из таблицы, она равна 385
Пример 2 – определение количества теплоты при остывании
Какое количество теплоты отдадут три литра воды при остывании от 100 до 20 градусов?
Теплоемкость воды (справочные данные) – 4200 (точнее – 4183)
Эту величину можно получить другим путем. Как известно, 1 калория – это количество теплоты, потребное для нагревания 1 г воды на 1 градус. В данном примере 3000 г воды нагревается на 80 градусов, отсюда 3000*80=240000 калорий. Поэтому калорию, как единицу измерения, удобно применять в теплотехнике там, где применяется водяное отопление.
Пример 3 — нагревание одновременно двух тел
Пусть имеется железный чайник массой 1 кг. В него налили воду объемом 2 литра (при нормальных условиях). Начальная температура чайника и воды — +25 градусов С. Какое количество теплоты потребуется, чтобы вскипятить воду?
В данном случае чайник и вода нагреваются одновременно, между ними существует постоянный теплообмен. Поэтому оба тела надо нагреть до одной и той же температуры, и
Пример 4 – смешивание воды с различной температурой
Приготовлена смесь из 800 граммов воды с температурой 25 градусов и 200 граммов воды с температурой 100 градусов. Полученная смесь имеет температуру 40 градусов. Какое количество теплоты получила первая (холодная) порция смеси? Какое количество теплоты отдала вторая (горячая) порция смеси?
Холодная порция воды нагрелась от 25 градусов до 40, и
Горячая порция остыла со 100 до 40 градусов, отсюда
Нагревательные элементы и энергопотребление
Для нагревания воды многие устройства используют нагревательные элементы. Они преобразуют электрическую энергию в тепловую, что позволяет повысить температуру воды до нужного уровня. Однако, для этого требуется определенное количество энергии.
Единицей измерения энергии является киловатт-час (кВт·ч), которая определяется как энергия, которую расходует устройство мощностью в 1 киловатт за 1 час.
При выборе нагревательного элемента для нагрева воды необходимо учесть его мощность. Чем выше мощность, тем быстрее будет происходить нагрев воды, однако и потребление электроэнергии будет соответственно выше.
Мощность нагревательного элемента обычно указывается на самом устройстве и указывается в ваттах (Вт) или киловаттах (кВт).
Для расчета количества энергии, необходимой для нагрева воды, можно использовать следующую формулу:
Энергия (кВт·ч) = мощность (кВт) х время (ч)
Например, если нагревательный элемент имеет мощность 2 кВт и работает в течение 3 часов, то энергопотребление будет равно:
2 кВт х 3 ч = 6 кВт·ч.
Обратите внимание, что эта формула упрощенная и не учитывает некоторые факторы, такие как потери энергии в процессе передачи, температурные потери и другие факторы, которые могут увеличить фактическое энергопотребление. Нагревательные элементы бывают различных типов и форм, включая тэны, нагревательные панели, нагревательные катушки и другие
Каждый из них имеет свои особенности и потребляет разное количество энергии. Поэтому при выборе нагревательного элемента необходимо обратить внимание на его мощность и энергопотребление
Нагревательные элементы бывают различных типов и форм, включая тэны, нагревательные панели, нагревательные катушки и другие. Каждый из них имеет свои особенности и потребляет разное количество энергии
Поэтому при выборе нагревательного элемента необходимо обратить внимание на его мощность и энергопотребление
Факторы, влияющие на потребление энергии
1. Температура воды: Чем выше температура воды, тем больше энергии требуется для ее нагрева.
Например, нагревание воды с комнатной температурой до кипения потребует больше энергии, чем нагревание воды с температурой в 40 градусов.
2. Объем воды: Чем больше объем воды, тем больше энергии потребуется для ее нагрева.
Например, нагревание большого бассейна потребует больше энергии, чем нагревание маленькой ванны.
3. Эффективность оборудования: Качество и состояние оборудования также влияют на потребление энергии.
Новое и эффективное оборудование потребляет меньше энергии в сравнении с устаревшими и неэффективными моделями.
4. Изоляция: Качество изоляции системы нагрева воды является важным фактором, влияющим на потребление энергии.
Хорошая изоляция поможет удерживать тепло внутри системы и снизить потребление энергии.
5. Использование вторичного тепла: Использование тепла, выделяемого другими системами или процессами,
таких как отопление или производство пара, может снизить потребление энергии для нагрева воды.
6. Способ нагрева: Различные способы нагрева воды, такие как использование газа, электричества, солнечной энергии
или тепловых насосов, могут потреблять разное количество энергии в зависимости от их эффективности и стоимости энергетических ресурсов.
7. Продолжительность работы: Время, в течение которого система нагрева воды работает, также влияет на ее энергопотребление.
Чем дольше система работает, тем больше энергии будет потреблено.
Примерное потребление энергии для нагрева воды разного объема и температуры
Объем воды (л)
Температура воды (°C)
Потребление энергии (кВт)
100
40
2.5
200
40
5
100
60
3.8
200
60
7.6
Физика
Пример 13. Рабочим веществом идеальной тепловой машины является идеальный одноатомный газ. Коэффициент полезного действия цикла 1–2–3–1 равен 30 %, а коэффициент полезного действия цикла 1–3–4–1 равен 40 %. Определить коэффициент полезного действия тепловой машины, работающей по циклу 1–2–3–4–1.
Решение. 1. Коэффициент полезного действия цикла 1–2–3–4–1 определяется формулой
η = A 1 2 + A 2 3 + A 3 4 + A 4 1 Q получ ⋅ 100 % ,
где A 12 — работа, совершаемая газом на участке 1–2; A 23 — работа, совершаемая газом на участке 2–3; A 34 — работа, совершаемая газом на участке 3–4; A 41 — работа, совершаемая газом на участке 4–1; Q получ — количество теплоты, полученной газом за цикл.
Запишем первое начало термодинамики для каждого участка:
участок 1–2 —
Q 12 = A 12 + ∆U 12 = A 12 + 1,5νR(T 2 − T 1) > 0,
где ΔU 12 — изменение внутренней энергии газа на участке 1–2, ∆U 12 = = 1,5νR(T 2 − T 1); ν — количество вещества (газа); R — универсальная газовая постоянная; T 1 — начальная температура газа на участке 1–2; T 2 — конечная температура газа на участке 1–2;
участок 2–3 —
Q 23 = A 23 + ∆U 23 = A 23 + 1,5νR(T 3 − T 2) > 0,
где ΔU 23 — изменение внутренней энергии газа на участке 2–3, ∆U 23 = = 1,5νR(T 3 − T 2); T 2 — начальная температура газа на участке 2–3; T 3 — конечная температура газа на участке 2–3;
участок 3–4 —
Q 34 = A 34 + ∆U 34 = A 34 + 1,5νR(T 4 − T 3) < 0,
где ΔU 34 — изменение внутренней энергии газа на участке 3–4; ∆U 34 = = 1,5νR(T 4 − T 3); T 3 — начальная температура газа на участке 3–4; T 4 — конечная температура газа на участке 3–4;
участок 4–1 —
Q 41 = A 41 + ∆U 41 = A 41 + 1,5νR(T 1 − T 4) < 0,
где ΔU 41 — изменение внутренней энергии газа на участке 4–1, ∆U 41 = = 1,5νR(T 1 − T 4); T 4 — начальная температура газа на участке 4–1; T 1 — конечная температура газа на участке 4–1.
Газ получает теплоту на участках 1–2 и 2–3, так как Q 12 и Q 23 являются положительными. Следовательно, полученное за цикл количество теплоты определяется формулой
Q получ = Q 1 2 + Q 2 3 = A 1 2 + 1,5 ν R ( T 2 − T 1 ) + A 2 3 + 1,5 ν R ( T 3 − T 2 ) .
После преобразований имеем:
Q получ = A 12 + A 23 + 1,5νR(T 3 − T 1).
Коэффициент полезного действия цикла
η = A 1 2 + A 2 3 + A 3 4 + A 4 1 A 1 2 + A 2 3 + 1,5 ν R ( T 3 − T 1 ) ⋅ 100 % .
Установим связь входящих в формулу величин с коэффициентами полезного действия на участках 1–2–3–1 и 1–3–4–1.
2. Коэффициент полезного действия тепловой машины, работающей по циклу 1–2–3–1.
Запишем первое начало термодинамики для каждого участка:
участок 1–2 —
Q 1 2 = A 1 2 + Δ U 1 2 = A 1 2 + 1,5 ν R ( T 2 − T 1 ) > 0 ;
участок 2–3 —
Q 2 3 = A 2 3 + Δ U 2 3 = A 2 3 + 1,5 ν R ( T 3 − T 2 ) > 0 ;
участок 3–1 —
Q 3 1 = A 3 1 + Δ U 3 1 = A 3 1 + 1,5 ν R ( T 1 − T 3 ) < 0 ,
где ΔU 31 — изменение внутренней энергии газа на участке 3–1, ∆U 31 = = 1,5νR(T 1 − T 3); T 3 — начальная температура газа на участке 3–1; T 1 — конечная температура газа на участке 3–1.
Коэффициент полезного действия цикла 1–2–3–1:
η 1 = A 1 2 + A 2 3 + A 3 1 A 1 2 + A 2 3 + 1,5 ν R ( T 3 − T 1 ) ⋅ 100 % .
3. Коэффициент полезного действия тепловой машины, работающей по циклу 1–3–4–1.
Запишем первое начало термодинамики для каждого участка:
участок 1–3 —
Q 1 3 = A 1 3 + Δ U 1 3 = A 1 3 + 1,5 ν R ( T 3 − T 1 ) > 0 ,
где ΔU 13 — изменение внутренней энергии газа на участке 1–3, ∆U 13 = = 1,5νR(T 3 − T 1); T 1– начальная температура газа на участке 1–3; T 3 — конечная температура газа на участке 1–3;
участок 3–4 —
Q 3 4 = A 3 4 + Δ U 3 4 = A 3 4 + 1,5 ν R ( T 4 − T 3 ) < 0 ;
участок 4–1 —
Q 4 1 = A 4 1 + Δ U 4 1 = A 4 1 + 1,5 ν R ( T 1 − T 4 ) < 0 .
Коэффициент полезного действия цикла 1–3–4–1:
η 2 = A 1 3 + A 3 4 + A 4 1 A 1 3 + 1,5 ν R ( T 3 − T 1 ) ⋅ 100 % .
Выражения для КПД образуют систему:
η = A 1 2 + A 2 3 + A 3 4 + A 4 1 A 1 2 + A 2 3 + 1,5 ν R ( T 3 − T 1 ) ⋅ 100 % , η 1 = A 1 2 + A 2 3 + A 3 1 A 1 2 + A 2 3 + 1,5 ν R ( T 3 − T 1 ) ⋅ 100 % , η 2 = A 1 3 + A 3 4 + A 4 1 A 1 3 + 1,5 ν R ( T 3 − T 1 ) ⋅ 100 % , }
которую необходимо решить относительно η.
Из второго уравнения системы следует
A 1 2 + A 2 3 = 1,5 ν R η 1 ( T 3 − T 1 ) − A 3 1 1 − η 1 ,
а из третьего —
A 1 3 + A 3 4 = 1,5 ν R η 2 ( T 3 − T 1 ) − A 1 3 ( 1 − η 2 ) ,
где η1 и η2 представлены в долях.
Подставим полученные уравнения в первое уравнение системы и преобразуем выражение
η = ( η 1 + η 2 − η 1 η 2 ) ( 1,5 ν R ( T 3 − T 1 ) + A 1 3 ) ( 1,5 ν R ( T 3 − T 1 ) − A 3 1 ) ⋅ 100 % .
С учетом
A 13 = −A 31
получим
η = ( η 1 + η 2 − η 1 η 2 ) ⋅ 100 % .
Вычислим:
η = ( 0,3 + 0,4 − 0,3 ⋅ 0,4 ) ⋅ 100 % = 58 % .
КПД тепловой машины, работающей по циклу 1–2–3–4–1, составляет 58 %.
Факторы, влияющие на количество теплоты
1. Масса вещества
Количество теплоты, передаваемое от одного тела к другому, зависит от их массы. Чем больше масса вещества, тем больше теплоты может быть передано или поглощено.
2. Температурная разница
Количество теплоты, передаваемое между телами, зависит от разницы их температур. Чем больше разница температур, тем больше теплоты будет передано.
3. Теплоемкость вещества
Каждое вещество имеет свою теплоемкость, которая означает, сколько теплоты нужно передать, чтобы повысить его температуру на 1 градус. Теплоемкость вещества зависит от его состава и физических свойств.
4. Изменение агрегатного состояния
При изменении агрегатного состояния вещества (например, при плавлении или кипении) требуется определенное количество теплоты. Это количество зависит от теплоты смешения и теплоты изменения фазы.
5. Теплопроводность
Теплопроводность вещества определяет скорость передачи тепла через него. Чем выше теплопроводность, тем быстрее будет передаться теплота.
6. Стереометрическая форма
Форма объектов также может влиять на количество теплоты. Например, удлиненные объекты теряют или поглощают больше теплоты вместе с теплопотерями или теплообменом окружающей среды.
Тепловой эффект реакции
Задание 82. Газообразный этиловый спирт С2Н5ОН можно получить при взаимодействии этилена С 2 Н 4 (г) и водяных паров. Напишите термохимическое уравнение этой реакции, предварительно вычислив ее тепловой эффект. Ответ: -45,76 кДж.Решение:
Уравнение реакции имеет вид:
С 2 Н 4 (г) + Н 2 О (г) = С2Н 5 ОН (г) ; = ?
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Рассчитаем тепловой эффект реакции, используя следствие из закона Гесса, получим:
= (С 2 Н 5 ОН) – = = -235,1 — = — 45,76 кДж
Уравнения реакций, в которых около символов химических соединений указываются их агрегатные состояния или кристаллическая модификация, а также числовое значение тепловых эффектов, называют термохимическими. В термохимических уравнениях, если это специально не оговорено, указываются значения тепловых эффектов при постоянном давлении Q p равные изменению энтальпии системы . Значение приводят обычно в правой части уравнения, отделяя его запятой или точкой c запятой. Приняты следующие сокращенные обозначения агрегатного состояния вещества: г
— газообразное, ж
— жидкое, к
Если в результате реакции выделяется теплота, то
С 2 Н 4 (г) + Н 2 О (г) = С 2 Н 5 ОН (г) ; = — 45,76 кДж.
Ответ:
— 45,76 кДж.
Задание 83.
Вычислите тепловой эффект реакции восстановления оксида железа (II) водородом, исходя из следующих термохимических уравнений:
а) ЕеО (к) + СО (г) = Fe (к) + СO 2 (г); = -13,18 кДж;б) СO (г) + 1/2O 2 (г) = СO 2 (г) ; = -283,0 кДж;в) Н 2 (г) + 1/2O 2 (г) = Н 2 O (г) ; = -241,83 кДж.Ответ: +27,99 кДж.
Решение:
Уравнение реакции восстановления оксида железа (II) водородом имеет вид:
ЕеО (к) + Н 2 (г) = Fe (к) + Н 2 О (г) ; = ?
= (Н2О) – [ (FeO)
Теплота образования воды определяется уравнением
Н 2 (г) + 1/2O 2 (г) = Н 2 O (г) ; = -241,83 кДж,
а теплоту образования оксида железа (II) можно вычислить, если из уравнения (б) вычесть уравнение (а).
=(в) — (б) — (а) = -241,83 – = +27,99 кДж.
Ответ:
+27,99 кДж.
Задание 84.
При взаимодействии газообразных сероводорода и диоксида углерода образуются пары воды и сероуглерод СS 2 (г) . Напишите термохимическое уравнение этой реакции, предварительно вычислите ее тепловой эффект. Ответ: +65,43 кДж.Решение:
г
— газообразное, ж
— жидкое, к
— кристаллическое. Эти символы опускаются, если агрегатное состояние веществ очевидно, например, О 2 , Н 2 и др.Уравнение реакции имеет вид:
2H 2 S (г) + CO 2 (г) = 2Н 2 О (г) + СS 2 (г); = ?
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствии е из закона Гесса:
= (Н 2 О) +(СS 2) – ;= 2(-241,83) + 115,28 – = +65,43 кДж.
2H 2 S (г) + CO 2 (г) = 2Н 2 О (г) + СS 2 (г) ; = +65,43 кДж.
Ответ:
+65,43 кДж.



























