Страницы
- Главная страница
- ОСНОВЫ ОБЩЕЙ ХИМИИ
- 1.1 Важнейшие классы неорганических веществ
- 2.1 Вещества. Атомы
- 2.2 Размеры атомов
- 2.3 Молекулы. Химические формулы
- 2.4 Простые и сложные вещества
- 2.5 Валентность элементов
- 2.6 Моль. Молярная масса
- 2.7 Закон Авогадро
- 2.8 Закон сохранения массы веществ
- 2.9 Вывод химических формул
- 3.1 Строение атома. Химическая связь
- 3.2 Строение атома
- 3.4 Строение электронной оболочки атома
- 3.5 Периодическая система химических элементов
- 3.6 Зависимость свойств элементов
- 3.7 Химическая связь и строение вещества
- 3.8 Гибридизация орбиталей
- 3.9 Донорно-акцепторный механизм образования
- 3.10 Степени окисления элементов
- 4.1 Классификация химических реакций
- 4.2 Тепловые эффекты реакций
- 4.3 Скорость химических реакций
- 4.4 Необратимые и обратимые реакции
- 4.5 Общая классификация химических реакций
- НЕОРГАНИЧЕСКАЯ ХИМИЯ
- 5.1 Растворы. Электролитическая диссоциация
- 5.2 Количественная характеристика состава растворов
- 5.3 Электролитическая диссоциация
- 5.4 Диссоциация кислот, оснований и солей
- 5.5 Диссоциация воды
- 5.6 Реакции обмена в водных растворах электролитов
- 5.7 Гидролиз солей
- 6.1 Важнейшие классы неорганических веществ
- 6.2 Кислоты, их свойства и получение
- 6.3 Амфотерные гидроксиды
- 6.4 Соли, их свойства и получение
- 6.5 Генетическая связь между важнейшими классами
- 6.6 Понятие о двойных солях
- 7.1 Металлы и их соединения
- 7.2 Электролиз
- 7.3 Общая характеристика металлов
- 7.4 Металлы главных подгрупп I и II групп
- 7.5 Алюминий
- 7.6 Железо
- 7.7 Хром
- 7.8 Важнейшие соединения марганца и меди
- 8.1 Неметаллы и их неорганические соединения
- 8.2 Водород, его получение
- 8.3 Галогены. Хлор
- 8.4 Халькогены. Кислород
- 8.5 Сера и ее важнейшие соединения
- 8.6 Азот. Аммиак. Соли аммония
- 8.7 Оксиды азота. Азотная кислота
- 8.8 Фосфор и его соединения
- 8.9 Углерод и его важнейшие соединения
- 8.10 Кремний и его важнейшие соединения
- ОРГАНИЧЕСКАЯ ХИМИЯ
- 9.1 Основные положения органической химии. Углеводороды
- 9.2 Электронные эффекты заместителей в органических соединениях
- 9.3 Предельные углеводороды (алканы)
- 9.3.1 Насыщенные УВ. Метан
- 9.4 Понятие о циклоалканах
- 9.5 Непредельные углеводороды
- 9.6 Диеновые углеводороды (алкадиены)
- 9.7 Алкины
- 9.8 Ароматические углеводороды
- 9.9 Природные источники углеводородов
- 10.1 Кислородсодержащие органические соединения
- 10.2 Фенолы
- 10.3 Альдегиды
- 10.4 Карбоновые кислоты
- 10.5 Сложные эфиры. Жиры
- 10.6 Понятие о поверхностно-активных веществах
- 10.7 Углеводы
- 11.1 Амины. Аминокислоты
- 11.2 Белки
- 11.3 Понятие о гетероциклических соединениях
- 11.4 Нуклеиновые кислоты
- 12.1 Высокомолекулярные соединения
- 12.2 Синтетические волокна
Хром
Хром относится к побочной подгруппе VI группы
Периодической системы. В природе существует в виде смеси 4-х
стабильных изотопов, из которых наиболее распространен
52Cr (мольная доля 83,76%). В земной коре массовая
доля хрома 8,310-3%, по
распространенности хром на 22-м месте. В природе встресается
только в виде соединений, наиболее распространенный минерал
хрома — хромит FeOCr2O3. Элемент хром открыт в 1797 г
французским химиком Вокленом.
Внешний
электронный уровень хрома имеет строение
3s23p63d54s1,
характерные степени окисления – от +1 до +6, наиболее устойчивы
+2,+3,+6.
Хром – металл серо-стального цвета, плотность
7,19 г/см3, плавится при 1890oС, кипит при
2660oС.
Технический хром очень
тверд (царапает стекло), чистый хром пластичен, легко поддается
ковке и прокатке.
Химические
свойства
При комнатной
температуре хром малоактивен, из простых веществ непосредственно
реагирует только со фтором. Выше 600oС реагирует с
кислородом:
Cr2O3
галогенами – в атмосфере хлора хром
сгорает:
CrCl3
Хром
растворяется в разбавленных соляной и серной кислотах, в
концентрированных серной и азотной кислотах хром пассивируется.
После обработки концентрированной азотной кислотой хром теряет
способность растворяться в кислотах.
Хром
взаимодействуе при нагревании с угарным газом СО, образуя легко
возгоняющийся карбонил хрома:
Cr(CO)6
Чистый хром получают методом алюмотермии:
Al2O3
Для
металлургии хром получают в виде сплава с железом (феррохром)
восстановлением хромистого железняка углем в электрической
печи:
2Cr + 4CO
Содержание хрома в
полученном сплаве доходит до 60%.
Хром
применяется:
1. в качестве легирующей
добавки к многочисленным сплавам на основе железа (например,
«нержавеющая» сталь).
2. в качестве
защитных покрытий, наносимых обычно гальваническими
методами.
Молярная масса элементов и соединений
Соединения — вещества, состоящие из различных атомов, которые химически связаны друг с другом. Например, приведенные ниже вещества, которые можно найти на кухне у любой хозяйки, являются химическими соединениями:
- соль (хлорид натрия) NaCl
- сахар (сахароза) C₁₂H₂₂O₁₁
- уксус (раствор уксусной кислоты) CH₃COOH
Молярная масса химических элементов в граммах на моль численно совпадает с массой атомов элемента, выраженных в атомных единицах массы (или дальтонах). Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении. Например, молярная масса воды (H₂O) приблизительно равна 1 × 2 + 16 = 18 г/моль.
Анодный процесс
В
электролитических ваннах для хромирования
используются нерастворимые аноды. Растворимые
аноды для хромирования не применяются.
Металлический хром растворяется на аноде
с выходом по току, в 7-8 раз превышающим
выход по току на катоде. При этом концентрация
ионов хрома в растворе непрерывно возрастает.
Значительная часть хрома переходит в
раствор в виде трехвалентных ионов, которые
на растворимом аноде не могут быть окислены
до шестивалентных.
При
электролизе растворов хромовой
кислоты на нерастворимом аноде
протекают два процесса: выделение
кислорода (4OH–→2e→O2+2H2O)
и окисление трехвалентного хрома до шестивалентного.
Часть кислорода, выделившегося в процессе
электролиза, окисляет свинец с образованием
темно-коричневой перекиси свинца. Хотя
свинцовые аноды считаются нерастворимыми,
все же с течением времени они разрушаются,
так как перекись свинца частично отделяется
от поверхности электрода и оседает на
дне ванны. Одновременно с этим свинец,
слабо взаимодействуя с хромовой кислотой,
образует на поверхности анода твердую,
плохо проводящую ток пленку хромовокислого
свинца.
Список
литературы
- Лайнер
В.И. Защитные покрытия металлов., М.
«Металлургия»., 1974г. - Плетнев Д.В.,
Бруснецова В.Н. Основы технологии
износостойких и антифрикционных покрытий.,
М: «Машиностроение»., 1968г. - Непрерывные
методы нанесения покрытий. Методические
указания для самостоятельной работы
по дисциплине «Теория и технология нанесения
покрытий»., сост. Полякова М.А., Магнитогорск,
2001г. - Твердые смазочные
покрытия. Сборник статей. Отв.ред., д-р
техн.наук Матвеевский Р.М., М: Наука, 1977г. - Хейфнец Л.И.
Электролиз никеля., М.: «Металлургия».,
1980г. - Гун Г.С., Чукин
М.В. и др. Упрочняющие и восстанавливающие
покрытия., Магнитогорск, 1982г. - Черкез М.Б.
Хромирование., Ленинград, «Машиностроение»,
1971г. - Бахматов
Ю.Ф., Голубчик Э.М. Конструирование
технологий нанесения покрытий на изделия
в метизной промышленности: Учеб. Пособие.
– Магнитогорск: МГТУ им. Г.И.Носова, 1999.
– 69с.
Химия водных растворов, в которых присутствует хромовая кислота
Оксид хрома CrO 3 быстро растворяется в воде. В водном растворе хром (VI) может существовать в различных ионных формах.
При pH> 6,5 или в щелочном растворе хром (VI) приобретает форму хромат-иона CrO 4 2 — желтого цвета.
Если pH понижен (1 <pH <6.5), хром (VI) в основном образует ион HCrO 4 — , который может димеризоваться до дихромат-иона Cr 2 O 7 2- , и раствор становится оранжевым. При pH от 2,5 до 5,5 преобладающими видами являются HCrO 4 — и Cr 2 O 7 2- .
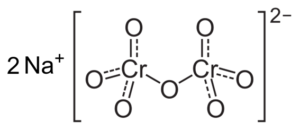
Балансы, возникающие в этих растворах при снижении pH, следующие:
CrO 4 2- (хромат-ион) + H + ⇔ HCrO 4 —
HCrO 4 — + H + ⇔ H 2 CrO 4 (хромовая кислота)
2HCrO 4 — ⇔ Cr 2 O 7 2- (дихромат-ион) + H 2 O
Этот баланс возникает только в том случае, если кислота, добавляемая для понижения pH, представляет собой HNO 3 или HClO 4 , потому что с другими кислотами образуются другие соединения.
Кислые дихроматные растворы — очень сильные окислители. Но в щелочных растворах хромат-ион гораздо менее окисляет.
Структура
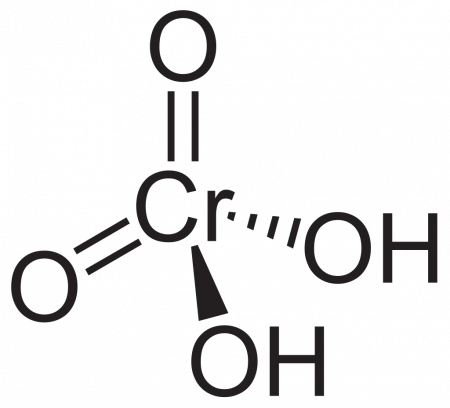
Молекула хромовой кислоты H 2 CrO 4 образована хромат-ионом CrO 4 2- и двумя присоединенными к нему ионами водорода H + . В хромат-ионе элемент Хром находится в степени окисления +6.
Пространственная структура хромат-иона тетраэдрическая, где хром находится в центре, а кислород занимает четыре вершины тетраэдра.
В хромовой кислоте каждый атом водорода находится вместе с кислородом. Из четырех связей хрома с атомами кислорода две двойные и две простые, так как к ним присоединены атомы водорода.
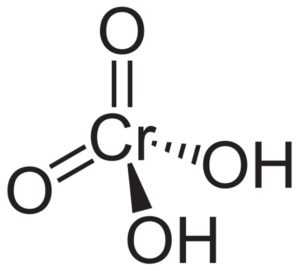
С другой стороны, оксид хрома CrO 3 имеет атом хрома в степени окисления +6, окруженный только тремя атомами кислорода.
Расчет молярной массы
Молярную массу рассчитывают так:
- определяют атомные массы элементов по таблице Менделеева;
- определяют количество атомов каждого элемента в формуле соединения;
- определяют молярную массу, складывая атомные массы входящих в соединение элементов, умноженные на их количество.
Например, рассчитаем молярную массу уксусной кислоты
Она состоит из:
- двух атомов углерода
- четырех атомов водорода
- двух атомов кислорода
Расчет:
- углерод C = 2 × 12,0107 г/моль = 24,0214 г/моль
- водород H = 4 × 1,00794 г/моль = 4,03176 г/моль
- кислород O = 2 × 15,9994 г/моль = 31,9988 г/моль
- молярная масса = 24,0214 + 4,03176 + 31,9988 = 60,05196 g/mol
Наш калькулятор выполняет именно такой расчет. Можно ввести в него формулу уксусной кислоты и проверить что получится.
Автор статьи: Anatoly Zolotkov
Моль
Все вещества состоят из атомов и молекул
В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ
Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро NA, если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц.
Постоянная Авогадро NA = 6.02214076×10²³ моль⁻¹. Число Авогадро — 6.02214076×10²³.
Другими словами моль — это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. Один моль чистого углерода-12 равен точно 12 г.
Плотность водных растворов солей, кислот и оснований
В таблице представлены значения отношения плотности водных растворов кислот, солей, оксидов, оснований к плотности воды при 15°С (999,9 кг/м 3 ). Например, плотность раствора соли NaCl равна 1008,5 кг/м 3 при концентрации соли в растворе 1% и 1146,2 кг/м 3 при концентрации 14%.
Плотность водных растворов кислот, солей и др. дана в зависимости от температуры и концентрации. Плотность относительно воды указана при температуре раствора в интервале от 15 до 20°С. Концентрация кислоты, щелочи, оксида или соли в растворе от 1 до 100%.
Значения плотности водных растворов кислот: мышьяковая кислота (ортомышьяковая кислота) H3AsO4, HBr, HCOOH, соляная кислота HCl, фтороводород HF, иодоводород HI, азотная кислота HNO3, перекись водорода H2O2, ортофосфорная кислота H3PO4, серная кислота H2SO4, H2SeO4, H2SiF6.
Значения плотности водных растворов солей: нитраты, хлориды, сульфаты, бромиды, йодиды, фосфаты, хроматы и др. Соли серебра, алюминия, бария, натрия, кадмия, кальция, меди, калия, никеля, олова, стронция, цинка, железа, селена, лития, магния, марганца, и других металлов: AgNO3, AlCl3, Al2(SO4)3, Al(NO3)3, BaBr2, BaCl2, BaI2, CdSO4, Cr2(SO4)3, Cu(NO3)2, медный купорос CuSO4, CUCl2, FeCl2, Fe(NO3)3, Fe2(SO4)3, CaBr2, CaCl2, CaI2, Ca(NO3)2, CdBr2, CdCl2, CdI2, Cd(NO3)2, FeSO4, KCl, KBr, K2CO3, KC2H3O2, K3CrO4, K2Cr2O7, KF, KHSO4, KI, KNO3, NaBr, NaBrO3, Na2CO2, NaCl, NaClO4, Na2Cr2O7, NaNO3, NaHSO4, Na2SO3, Na2SO4, Na2S2O3, NiCl2, Ni(NO3)2, NiSO4, Pb(NO3)2, SO2, SnCl2, SnCl4, SrBr2, SrI2, ZnBr2, ZnCl4, ZnI2, Zn(NO3)2, ZnSO4, Sr(NO3)2, LiBr, LiCl, LiI, MgBr, MgCl2, MgI2, Mg(NO3)2, MgSO4, MgBr2, MnCl2, Mn(No3)2, MnSO4, NH3, N2H4, NH4Cl, NH4I, NH4NO3, (NH4)2SO4.
Значения плотности водных растворов оксидов: раствор оксида хрома CrO2.
Значения плотности водных растворов оснований (щелочи): NaOH, KOH.
Катодный процесс
Процесс
хромирования в хромовокислых электролитах
протекает в результате восстановления
на катоде сложного многовалентного аниона
при одновременном образовании соединений
хрома промежуточной валентности. При
этом на катоде совместно протекает несколько
реакций.
В
присутствии анионов пленка на катоде
не разрыхляется, а наоборот уплотняется.
При этом осаждение рома на катоде происходит
за счет восстановления шестивалентных
ионов хрома, входящих в состав самой пленки.
В хромовокислых растворах с добавкой
серной кислоты при заданном постоянном
значении потенциала катодная плотность
тока, имевшая в начальный момент относительно
большую величину, через короткий промежуток
времени, резко снижалась. Такое сильное
торможение электрохимического процесса
является результатом образования на
поверхности катода плотной пленки из
продуктов реакции. При выключении тока
пленка растворялась, а после включения
наблюдалось повторное явление. В растворах
хромового ангидрида, не содержащих серной
кислоты, величина начальной плотности
тока выше, а снижение ее во времени менее
резкое. Такое изменение плотности тока
свидетельствует об уплотнении коллоидной
пленки на катоде в присутствии серной
кислоты. Образование пленки на катоде
вызывается смещение потенциала катода
в отрицательную область. Благодаря этому
наряду с разрядом ионов водорода становится
возможным восстановление шестивалентных
соединений хрома до металла и трехвалентного
хрома.
Установлено,
что при относительно невысоких
значениях потенциалов, при которых
не происходит выделения металлического
хрома с увеличением концентрации
ионов SO42+ скорость Cr6+
до Cr3+ резко возрастает и определяется
предельным током реакции Cr6+ → Cr3+.
Эта реакция протекает наиболее легко
и лишь при ее торможении в области отрицательных
потенциалов создаются благоприятные
условия для осуществления Cr6+ →
Cr3+. Следует отметить положительное
влияние пленки, образующейся на поверхности
катода, которая несколько тормозит реакцию
разряда ионов водорода. В вопросе о вреде
или пользе пленки общим является мнение
о том, что в процессе электролиза на поверхности
катода образуется фазовая пленка из соединений
высшей и низшей валентности хрома. На
катоде происходит непосредственное восстановление
шестивалентных ионов хрома до металла.
При химической конверсии
Хромовая кислота используется в процессах нанесения покрытий на металл путем химического превращения.
Во время этого процесса металлы погружаются в растворы хромовой кислоты. Это реагирует и частично растворяет поверхность, осаждая тонкий слой сложных соединений хрома, которые взаимодействуют с основным металлом.
Этот процесс называется конверсионным хромированием или конверсионным хромированием.
Металлы, которые обычно подвергаются конверсионному хромированию, представляют собой различные типы стали, такие как углеродистая сталь, нержавеющая сталь и сталь с цинковым покрытием, а также различные цветные металлы, такие как сплавы магния, сплавы олова, алюминиевые сплавы, медь. , кадмий, марганец и серебро.
Эта обработка обеспечивает устойчивость к коррозии и блеск металла. Чем выше pH процесса, тем выше устойчивость к коррозии. Температура ускоряет кислотную реакцию.
Могут применяться покрытия различных цветов, такие как синий, черный, золотой, желтый и прозрачный. Он также обеспечивает лучшую адгезию металлической поверхности к краскам и клеям.
Ссылки
- Коттон, Ф. Альберт и Уилкинсон, Джеффри. (1980). Продвинутая неорганическая химия. Четвертое издание. Джон Вили и сыновья.
- Национальная медицинская библиотека США. (2019). Хромовая кислота. Получено с: pubchem.ncbi.nlm.nih.gov
- Вегман, Р.Ф. и Ван Твиск, Дж. (2013). Алюминий и алюминиевые сплавы. 2.5. Процесс анодирования хромовой кислотой. В методах подготовки поверхности для склеивания (второе издание). Восстановлено с sciencedirect.com.
- Вегман, Р.Ф. и Ван Твиск, Дж. (2013). Магний. 6.4. Получение магния и магниевых сплавов процессами обработки хромовой кислотой. В методах подготовки поверхности для склеивания (второе издание). Восстановлено с sciencedirect.com.
- Грот, В. (2011). Приложения. 5.1.8. Регенерация хромовой кислоты. Во фторированных иономерах (второе издание). Восстановлено с sciencedirect.com.
- Свифт, К.Г. и Букер, Д.Д. (2013). Поверхностные инженерные процессы. 9,7. Хромирования. В Справочнике по выбору производственного процесса. Восстановлено с sciencedirect.com.
- Поулссон, AHC et al. (2019). Методы модификации поверхности PEEK, включая плазменную обработку поверхности. 11.3.2.1. Поверхностное травление. В Справочнике по биоматериалам PEEK (второе издание). Восстановлено с sciencedirect.com.
- Вестхаймер, FH (1949). Механизмы окисления хромовой кислоты. Химические обзоры 1949 г., 45, 3, 419-451. Восстановлено с pubs.acs.org.
- Тан, HKS (1999). Удаление хромовой кислоты анионным обменом. Канадский журнал химической инженерии, том 77, февраль 1999 г. Получено с onlinelibrary.wiley.com.
- Кабир, М.М. и др. (2018). Выделение и характеристика бактерий, восстанавливающих хром (VI), из сточных вод кожевенных заводов и твердых отходов. Всемирный журнал микробиологии и биотехнологии (2018) 34: 126. Восстановлено с ncbi.nlm.nih.gov.
Молекулярная хромовая кислота
диаграмма преобладания
Молекулярная хромовая кислота H 2 CrO 4 имеет много общего с серной кислотой, H 2SO4. Только серная кислота может быть отнесена к списку 7 сильных кислот. Из-за законов, относящихся к концепции «энергии ионизации первого порядка», первый протон теряется легче всего. Он ведет себя очень похоже на депротонирование серной кислоты. Поскольку процесс титрования поливалентной кислотой и основанием включает более одного протона (особенно, когда кислота является исходным веществом, а основание — титрантом), протоны могут выходить из кислоты только по одному. Следовательно, первый шаг выглядит следующим образом:
- H2CrO 4 ⇌ + H
pKa для равновесия недостаточно хорошо охарактеризован. Сообщаемые значения варьируются от -0,8 до 1,6. Значение при нулевой ионной силе трудно определить, потому что половинная диссоциация происходит только в очень кислом растворе, примерно при pH 0, то есть при концентрации кислоты примерно 1 моль-дм. Еще одна сложность заключается в том, что ион имеет явную тенденцию к димеризации с потерей молекулы воды с образованием дихромат-иона :
- 2 ⇌ + H 2 O log K D = 2,05.
Кроме того, дихромат может быть протонирован:
- ⇌ + H pK = 1,8
Значение pK для этой реакции показывает, что им можно пренебречь при pH>4.
Потеря второго протона происходит в диапазоне pH 4–8, что делает ион слабой кислотой.
Молекулярная хромовая кислота в принципе может быть получена добавлением триоксида хрома к воде (см. производство серной кислоты ).
- CrO 3 + H 2 O ⇌ H 2 CrO 4
, но на практике при дегидратации молекулярной хромовой кислоты происходит обратная реакция. Вот что происходит при добавлении концентрированной серной кислоты к раствору дихромата. Сначала цвет меняется с оранжевого (дихромат) на красный (хромовая кислота), а затем из смеси выпадают темно-красные кристаллы триоксида хрома без дальнейшего изменения цвета. Цвета обусловлены переходами LMCT.
Триоксид хрома представляет собой ангидрид молекулярной хромовой кислоты. Это кислота Льюиса, которая может взаимодействовать с основанием Льюиса, таким как пиридин, в неводной среде, такой как дихлорметан (реагент Коллинза ).
Применение
Растворы хромовой кислоты используют при электролитическом хромировании и получении хрома электролизом. Хромовая кислота является промежуточным веществом при хромировании, а также используется в керамической мураве и в цветных композициях стекла. Поскольку раствор хромовой кислоты в серной (также известная как «сульфохромовая кислота») является мощным окислителем, эта смесь может быть использована для очистки лабораторной посуды, или для растворения нерастворимых органических остатков.
Так же растворы хромовой кислоты являются качественным реактивом на серебро, наносится тонким слоем на метал.В случае, если изделие сделано из серебра, на нем в месте контакта с реактивом возникает кроваво-красное пятно. Чем чище серебро тем интенсивнее окраска.
Хромовую кислоту используют для производства:
- металлического хрома высокой чистоты,
- катализаторов,
- электролитического хрома,
- сверхтвердых материалов,
- в производстве литья в составе формовочных и стержневых смесей,
- для процессов хромирования, хроматирования и пассивирования,
- для процессов травления.
хромовая кислота аскорбиновая, хромовая кислота во, хромовая кислота геалуроновая, хромовая кислота фолиевая
Ангидрид хромовый представляет собой твердое вещество в виде чешуек или гранул. Цвет от светло- до темно-малинового. Сильно ядовит! В воде легко растворим, гигроскопичен. Сильный окислитель, разрушает органические вещества. Не горюч. Раздражающе действует на кожу, глаза и слизистые оболочки.
Применение
В промышленном производстве в качестве окислителя.
Для травления и хромирования металлов.
Для получения хрома.
В производстве органических красителей.
В производстве литья в составе формовочных или стержневых смесей.
Упаковка
Технический хромовый ангидрид упаковывают в стальные барабаны для химических продуктов.
Транспортировка
Хромовый ангидрид транспортируют всеми видами транспорта (кроме авиации) в крытых транспортных средствах в сооветствии с правилами перевозки опасных грузов.
Хранение
Технический хромовый ангидрид хранят в закрытом складском помещении в неповрежденной упаковке. Контейнеры хранят на контейнерных площадках. Хранение продукта вместе с горючими веществами не допускается. Ангидрид хромовый упаковывают в плотно закрывающиеся стальные барабаны по 50 кг (вес нетто до 150 кг). Хранить в закрытых помещениях. Беречь от сырости и от нагревания.
Гарантийный срок хранения
продукта — 1 год со дня изготовления.
Технические характеристики
|
Показатели качества |
Марка А |
Марка Б |
Марка В |
|
Массовая доля хромового ангидрида (CrO 3), % не менее |
99,7 |
98,8 |
98,0 |
|
Массовая доля веществ, нерастворимых в воде, % не более |
0,02 |
0,05 |
не нормируется |
|
Массовая доля сульфатов (SO 4), % не более |
0,06 |
0,18 |
не нормируется |
|
Массовая доля натрия (Na), % не более |
0,05 |
не нормируется |
не нормируется |
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см 3 Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO 3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO 3):
CrO 3 (недост.) + H 2 O = H 2 CrO 4 ,
или дихромовая кислота (при избытке CrO 3):
2CrO 3 + H 2 O = H2Cr 2 O 7 .
При взаимодействии CrO 3 со щелочами образуются хроматы:
CrO 3 + 2KOH = K2CrO 4 + H 2 O.
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
4CrO 3 = 2Cr 2 O 3 + 3O 2 .
Как и все соединения Cr(VI), CrO 3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет йод, серу, фосфор, уголь, например:
4CrO 3 + 3S = 2Cr 2 O 3 + 3SO 2 .
Безопасность
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. При попадании на кожу он вызывает сильнейшие раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Весьма опасно вдыхание паров хромового ангидрида.
Для хранения его применяется стеклянная или пластиковая герметичная посуда, и исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
Основные свойства и виды опасности
Хромовая кислота

| Хромовая кислота | ||
|---|---|---|
|
||
| Хим. формула | H2CrO4 | |
| Состояние | твердые красные пласты | |
| Молярная масса | 118.00958 г/моль | |
| Плотность | 1,201 г/см³ | |
| Температура | ||
| • плавления | 197 °C | |
| • разложения | 387 ± 1 °F и 482 ± 1 °F | |
| Растворимость | ||
| • в воде | 166.66 г/100 мл | |
| Рег. номер CAS | 7738-94-5 | |
| PubChem | 24425 | |
| Рег. номер EINECS | 231-801-5 | |
| SMILES | ||
| ChEBI | 33143 | |
| ChemSpider | 22834 | |
| ЛД50 | 51 мг/кг | |
| Токсичность | Высокотоксичное и канцерогенное вещество | |
| Пиктограммы ECB | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. |
Хромовая кислота — кристаллическое вещество красного цвета. Химическая формула H2CrO4. В водных растворах имеет жёлтый цвет. Выделена в свободном состоянии при охлаждении насыщенных водных растворов хромата.
Соли хромовой кислоты называются хроматами. Сильный окислитель. Токсична, канцерогенна.