Пластичность и хрупкость
Есть ряд материалов, которые претерпевают деформацию при небольшом внешнем воздействии. Это свойство пластичности, которое отличает аморфные твердые тела.
Другая группа материалов – это материалы, способные разрушиться при незначительном воздействии. Это свойство хрупкости, оно на практике оказывается более востребованным, чем упругость и пластичность. Одним из наиболее хрупких материалов является фарфор. Нам известно, что будет с фарфоровым предметом, если уронить его с высоты.
Один и тот же материал условно способен приобретать упругость или пластичность зависимо от возникающих напряжений. У разных материалов свой предел прочности: при определенной нагрузке происходит разрыв материала. В таком случае говорят, что напряжение в этом момент достигло своего максимального значения. Эта величина зависит от материала и качества его обработки.
Что такое кристаллы
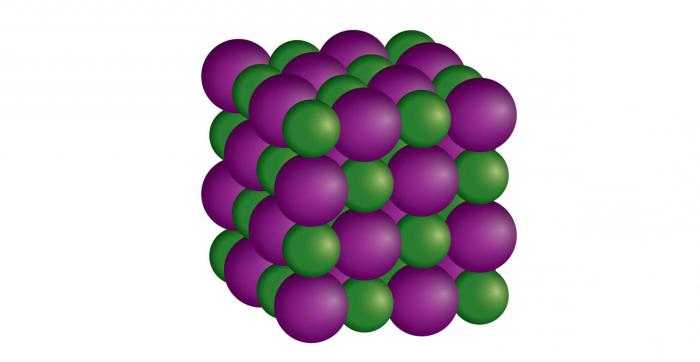
Кристаллы — это твердые тела с расположенными в определенном порядке частицами. Каждому соответствует своя структура. Его атомы образуют трехмерно-периодическую укладку, называемую кристаллической решеткой. Твердые вещества обладают различной симметрией структуры. Кристаллическое состояние твердого тела считается устойчивым, поскольку имеет минимальное количество потенциальной энергии.
Подавляющее большинство твердых состоит из огромного числа беспорядочно ориентированных отдельных зерен (кристаллитов). Такие вещества называют поликристаллическими. К ним относят технические сплавы и металлы, а также множество горных пород. Монокристаллическими называют одиночные природные или синтетические кристаллы.
Чаще всего такие твердые тела образуются из состояния жидкой фазы, представленного расплавом или раствором. Иногда их получают и из газообразного состояния. Этот процесс называют кристаллизацией. Благодаря научно-техническому прогрессу процедура выращивания (синтеза) различных веществ получила промышленный масштаб. Большинство кристаллов имеет естественную форму в виде Их размеры бывают самыми разными. Так, природный кварц (горный хрусталь) может весить до сотен килограммов, а алмазы — до нескольких грамм.
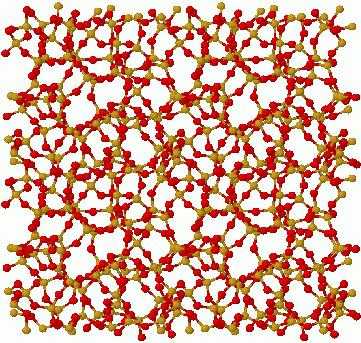
В аморфных твердых телах атомы находятся в постоянном колебании вокруг хаотически находящихся точек. В них сохраняется определенный ближний порядок, но отсутствует дальний. Это обусловлено тем, что их молекулы расположены на расстоянии, которое можно сравнить с их размером. Наиболее часто встречающимся в нашей жизни примером такого твердого вещества является стеклообразное состояние. часто рассматриваются как жидкость с бесконечно большой вязкостью. Время их кристаллизации иногда так велико, что и вовсе не проявляется.
Именно вышеперечисленные свойства данных веществ делают их уникальными. Аморфные твердые тела считаются нестабильными, поскольку со временем могут перейти в кристаллическое состояние.
Молекулы и атомы, из которых состоит твердое вещество, упакованы с большой плотностью. Они практически сохраняют свое взаимоположение относительно иных частиц и держатся вместе благодаря межмолекулярному взаимодействию. Расстояние между молекулами твердого вещества в различных направлениях именуют параметром кристаллической решетки. Структура вещества и ее симметричность определяют множество свойств, таких как электронная зона, спайность и оптика. При воздействии на твердое вещество достаточно большой силы эти качества могут быть в той или иной степени нарушены. При этом твердое тело поддается остаточной деформации.
Атомы твердых тел совершают колебательные движения, которыми обусловлено обладание ими тепловой энергией. Поскольку они ничтожно малы, их можно наблюдать только при лабораторных условиях. твердого вещества во многом влияет на его свойства.
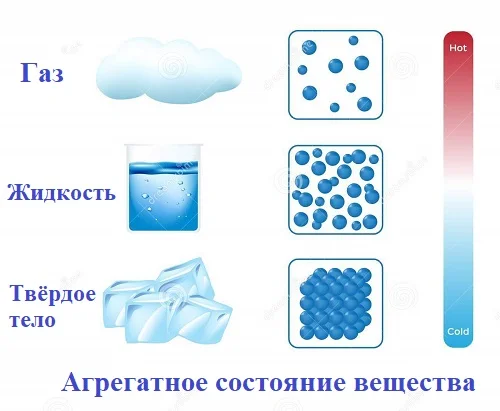
Три агрегатных состояния
Какое вещество на Земле самое привычное и распространенное? Конечно, вода. Вода встречается повсюду, причем в разном виде (лед или снег, жидкость, пар). Это агрегатные состояния воды.

Абсолютно все вещества меняют внешний вид и свойства. Происходит это при определенной для каждого вещества температуре. Кислород, если его охладить до – 183о С бывает голубой жидкостью, а железо кипит при 2750о С. Непривычно, но это так.
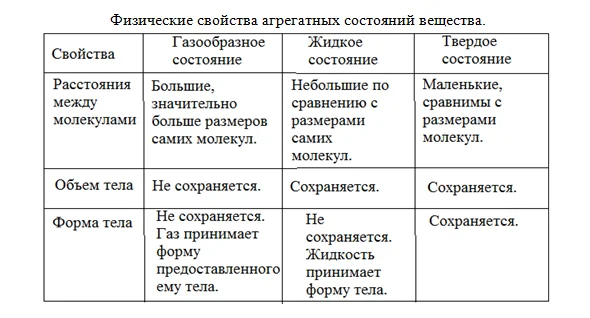
Каковы же свойства и отличие агрегатных состояний?
Например, воздух. Пусть в квартире в одну из комнат воздух не попал. Такого не может быть. Воздух – смесь нескольких газов, но, как и любой газ, занимает всю емкость предоставленную ему. Расстояние между соседними молекулами газа или пара намного больше самих молекул. Поэтому взаимодействие между молекулами не существует. Они разлетаются по всему пространству, которое им предоставляется (в квартире все комнаты заполняется воздухом).
На больших расстояниях молекулы легко можно сближать, силы отталкивания мешать не будут. Значит, газы легко сжимаемы. Воздушный шарик легко сжимается. Камеру велосипеда сжать труднее, а баллон автомобиля тем более. Чем больше молекул газа содержится в единице объема (а в камеры велосипеда и автомобиля их накачивают насосами специально), тем они плотнее друг к другу, а значит, и сблизить их можно лишь чуть-чуть.
Молекулы жидкости располагаются близко. Они не летают свободно, как в газе, но и не стоят на месте, а как будто топчутся, затем перескакивают на небольшое расстояние, затем снова меняют место, и так без конца.
Почему жидкости почти несжимаемы? Стоит сблизить молекулы, как сразу начинает действовать отталкивание. Вода текуча и принимает форму сосуда, где находится. Если ее вылить на пол, то растечется по нему. Но зато, жидкость в разных по форме сосудах имеет одинаковый объем. Если литровую банку молока перелить в трехлитровую, то в ней так и останется один литр молока.
Внутри твердого вещества молекулы располагаются на своих, строго определенных местах. Это вовсе не значит, что они не движутся. Они постоянно колеблются, участвуя в тепловом движении. Такое расположение называется кристаллической решеткой, а тела – кристаллами. Форма и объем у твердых тел сохраняются (не разлетаются и не растекаются).
 (Источник)
(Источник)
Для наглядности три возможных состояния вещества можно сравнить с людьми. Люди, бродящие по базару, кто куда хочет – «газ», люди на митинге – «жидкость», участники парада – «твердое тело».
Греческий ученый Эмпедокл (врач, поэт, музыкант, основатель Сицилийской медицинской школы) в V веке до нашей эры впервые выдвинул такую интересную гипотезу: весь мир состоит из воздуха, воды, земли и огня.
Первые три элемента соответствуют трем агрегатным состояниям.
А как быть с огнем? Огонь – это четвертое состояние вещества, называется словом «плазма». (Физические свойства плазмы сложны, изучается это понятие позднее).

Итак:
- Вещество может находиться в трех агрегатных состояниях: твердом, жидком и газообразном. Плазма — это отдельное состояние вещества;
- При определенных условиях тело может переходить из одного состояния в другое;
- Агрегатное состояние определяется движением и взаимодействие молекул вещества.
Свойства твердых веществ
Что нам известно на сегодняшний день? Ученые давно изучают свойства твердого состояния вещества. При воздействии на него температур изменяется и оно. Переход такого тела в жидкость называют плавлением. Трансформация твердого вещества в газообразное состояние называется сублимацией. При понижении температуры происходит кристаллизация твердого тела. Некоторые вещества под действием холода переходят в аморфную фазу. Этот процесс ученые называют стеклованием.
При изменяется внутренняя структура твердых тел. Наибольшую упорядоченность она приобретает при понижении температуры. При атмосферном давлении и температуре Т > 0 К любые вещества, существующие в природе, затвердевают. Только гелий, для кристаллизации которого нужно давление в 24 атм, составляет исключение из этого правила.
Твердое состояние вещества придает ему различные физические свойства. Они характеризуют специфическое поведение тел под воздействием определенных полей и сил. Эти свойства подразделяют на группы. Выделяют 3 способа воздействия, соответствующие 3 видам энергии (механической, термической, электромагнитной). Соответственно им существует 3 группы физических свойств твердых веществ:
- Механические свойства, связанные с напряжением и деформацией тел. По этим критериям твердые вещества делят на упругие, реологические, прочностные и технологические. В покое такое тело сохраняет свою форму, но оно может изменяться под действием внешней силы. При этом его деформация может быть пластической (начальный вид не возвращается), упругой (возвращается в первоначальную форму) или разрушительной (при достижении определенного порога происходит распад/разлом). Отзыв на прилагаемое усилие описывают модулями упругости. Твердое тело сопротивляется не только сжатию, растяжению, но и сдвигам, кручению и изгибам. Прочностью твердого тела называют его свойство сопротивляться разрушению.
- Термические, проявляющиеся при воздействии тепловых полей. Одно из самых важных свойств — температура плавления, при которой тело переходит в жидкое состояние. Оно отмечается у кристаллических твердых веществ. Аморфные тела обладают скрытой теплотой плавления, поскольку их переход в жидкое состояние при повышении температуры происходит постепенно. По достижении определенной теплоты аморфное тело теряет упругость и приобретает пластичность. Это состояние означает достижение им температуры стеклования. При нагревании происходит деформация твердого тела. Причем оно чаще всего расширяется. Количественно это состояние характеризуется определенным коэффициентом. Температура тела влияет на такие механические характеристики, как текучесть, пластичность, твердость и прочность.
- Электромагнитные, связанные с воздействием на твердое вещество потоков микрочастиц и электромагнитных волн большой жесткости. К ним условно относят и радиационные свойства.

Как проявляется тепловое движение в твердых телах
Тепловое движение в твердых телах происходит за счет кинетической энергии, которую получают молекулы от своей внутренней энергии. Молекулы твердого тела постоянно вибрируют, колеблятся и двигаются вокруг своих положений равновесия.
Тепловое движение в твердых телах имеет два основных проявления — это тепловое расширение и возможность передачи тепла. При нагревании твердого тела, его молекулы начинают двигаться с большей амплитудой, в результате чего происходит расширение самого тела. Это явление называется тепловым расширением и является следствием теплового движения молекул внутри твердого тела.
Также тепловое движение в твердом теле позволяет ему обменяться теплом с окружающей средой. Молекулы твердого тела, колеблясь, передают свою кинетическую энергию соседним молекулам, и тем самым энергия распространяется по всему телу. Этот процесс называется теплопроводностью и позволяет твердым телам согреваться или остывать в зависимости от теплового потока.
Таким образом, тепловое движение в твердых телах является неотъемлемым свойством их структуры. Оно проявляется через вибрацию и колебания молекул, обеспечивает тепловое расширение и возможность передачи тепла. Понимание этого явления позволяет более глубоко изучать свойства и поведение твердых тел.
Молекулярная структура твердых тел
Молекулярная структура твердых тел определяет их физические и химические свойства и играет ключевую роль в понимании особенностей теплового движения молекул. В отличие от жидкостей и газов, твердые тела обладают регулярным и упорядоченным расположением своих молекул.
Молекулы в твердых телах могут быть организованы в различные структуры, включая кристаллические и аморфные. Кристаллические твердые тела имеют атомы или молекулы, упорядоченно расположенные в пространстве согласно определенным правилам симметрии. Они обладают характерными кристаллическими решетками, которые обеспечивают продолжительность и устойчивость структуры. Аморфные твердые тела, напротив, имеют беспорядочную структуру и отсутствуют характерные кристаллические решетки.
Молекулярный состав и упорядоченность молекул в твердых телах определяют их свойства. Различные молекулярные структуры могут обладать различными термодинамическими, механическими и электрическими свойствами.
Одной из особенностей молекулярной структуры твердых тел является возможность колебаний молекул вокруг своих равновесных положений. Эти колебания называются фононами и играют важную роль в передаче тепла через твердое тело. Также молекулярная структура влияет на тепловую расширяемость, прочность и оптические свойства твердых тел.
Твердотельная физика и химия изучают молекулярную структуру твердых тел, исследуя их кристаллическую и аморфную структуру, а также взаимодействие между молекулами. Это позволяет получить более глубокое понимание физических и химических процессов, происходящих в твердых телах, и разрабатывать новые материалы с желаемыми свойствами.
Взаимодействие молекул в твердых телах
В твердых телах молекулы взаимодействуют друг с другом различными способами. Это взаимодействие определяет особенности теплового движения молекул в твердых телах.
Одним из основных видов взаимодействия молекул является электростатическое взаимодействие. Молекулы в твердом теле обладают электрическим зарядом, который может быть положительным или отрицательным. Взаимодействие молекул происходит за счет притяжения и отталкивания этих зарядов.
На тепловое движение молекул в твердых телах также влияет взаимодействие молекул через твердые связи. Молекулы в твердом теле могут быть связаны между собой с помощью химических связей или слабых взаимодействий, таких как водородные связи или взаимодействия Ван-дер-Ваальса. Эти связи между молекулами могут быть достаточно сильными и не позволять молекулам свободно перемещаться.
За счет взаимодействия молекул в твердых телах возникает регулярная упорядоченность структуры, что делает твёрдое тело прочным и устойчивым. Поэтому твердые тела обладают определенной формой и объемом при данной температуре и давлении.
Молекулы беспорядочно движутся
2) Молекулы находятся в непрерывном беспорядочном (тепловом) движении.
Вид теплового движения (поступательное, колебательное, вращательное) молекул зависит от характера их взаимодействия и изменяется при переходе вещества из одного агрегатного состояния в другое. Интенсивность теплового движения зависит и от температуры тела.
Приведем некоторые из доказательств беспорядочного (хаотического) движения молекул: а) стремление газа занять весь предоставленный ему объем; б) диффузия; в) броуновское движение.
Диффузия
Диффузия — самопроизвольное взаимное проникновение молекул соприкасающихся веществ, приводящее к выравниванию концентрации вещества по всему объему. При диффузии молекулы граничащих между собой тел, находясь в непрерывном движении, проникают в межмолекулярные промежутки друг друга и распределяются между ними.
Диффузия проявляется во всех телах — в газах, жидкостях, твердых телах, но в разной степени.
Диффузию в газах можно обнаружить, если, например, сосуд с пахучим газом открыть в помещении. Через некоторое время газ распространится по всему помещению.
Диффузия в жидкостях происходит значительно медленнее, чем в газах
Например, если в стакан налить сначала слой раствора медного купороса, а затем очень осторожно добавить слой воды и оставить стакан в помещении с неизменной температурой, то через некоторое время исчезнет резкая граница между раствором медного купороса и водой, а через несколько дней жидкости перемешаются
Диффузия в твердых телах происходит еще медленнее, чем в жидкостях (от нескольких часов до нескольких лет). Она может наблюдаться только в хорошо отшлифованных телах, когда расстояния между поверхностями отшлифованных тел близки к межмолекулярному расстоянию (10-8 см). При этом скорость диффузии увеличивается при повышении температуры и давления.
Диффузия играет большую роль в природе и технике. В природе благодаря диффузии, например, осуществляется питание растений из почвы. Организм человека и животных всасывает через стенки пищеварительного тракта питательные вещества. В технике с помощью диффузии, например, поверхностный слой металлических изделий насыщается углеродом (цементация) и т.д.
Разновидностью диффузии является осмос — проникновение жидкостей и растворов через пористую полупроницаемую перегородку.
Броуновское движение
Броуновское движение открыто в 1827 г. английским ботаником Р. Броуном, теоретическое обоснование с точки зрения MKT дано в 1905 г. А. Эйнштейном и М. Смолуховским.
Броуновское движение — это беспорядочное движение мельчайших твердых частиц, «взвешенных» в жидкостях (газах).
«Взвешенные» частицы — это частицы, плотность вещества которых сравнима с плотностью среды, в которой они находятся. Такие частицы находятся в равновесии, и малейшее внешнее воздействие на нее приводит к их движению.
Для броуновского движения характерно следующее:
- броуновские частицы совершают непрерывное хаотическое движение, интенсивность которого зависит от температуры и от размеров броуновской частицы;
- траектория движения броуновской частицы очень сложная, не зависит от природы вещества частиц и внешних условий.
Рис. 2
На рисунке 2 показаны положения броуновской частицы через каждые 30 с, а на врезке — положения этой частицы на участке АВ, зафиксированные через каждую секунду. Эти положения соединены прямыми линиями. Траектория же частицы еще более сложная;
- броуновское движение наблюдается в жидкостях и газах.
Причинами броуновского движения являются:
- тепловое хаотическое движение молекул среды, в которой находится броуновская частица;
- отсутствие полной компенсации ударов молекул среды об эту частицу с различных сторон, так как движение молекул носит случайный характер.
Движущиеся молекулы жидкости при столкновении с какими-либо твердыми частицами передают им некоторое количество движения. Случайно с одной стороны о частицу ударит заметно большее число молекул, чем с другой, и частица придет в движение.
Если частица достаточно велика, то число молекул, налетающих на нее со всех сторон, чрезвычайно велико, их удары в каждый данный момент компенсируются, и такая частица практически остается неподвижной.
Что такое тепло?
Начнем с вопроса, который настолько же прост, насколько и сложен: что такое тепло?
Тепло — это физическая энергия, образующаяся в результате неупорядоченного движения частиц тела (атомов, молекул и т.д.) и проявляющаяся в нагревании тела.
Такое определение не сразу стало известно людям. Например, предполагалось, что тепло — это невидимая, неощутимая жидкость, которая течет через физические тела. И чем больше объем этой жидкости, тем горячее тело. Конечно, эта гипотеза не подтвердилась.
Позже ученые изучили поведение молекул при нагревании или охлаждении тела. При повышении температуры скорость молекул увеличивается, и они чаще сталкиваются друг с другом. Это увеличивает потенциальную и кинетическую энергию, а значит и внутреннюю энергию, что выражается в буквальном нагревании тела. Это хаотичное движение молекул называется тепловым движением.
Тепловое движение — это процесс хаотического движения частиц, составляющих материю.
Если скорость молекул увеличивается при повышении температуры, то можно предположить, что скорость уменьшается при понижении температуры. Но можно ли полностью остановить движение? До какой температуры должно быть охлаждено тело в таком случае?
Для этого тело должно быть охлаждено до абсолютного нуля по шкале Кельвина, что соответствуе т-273,15 °C ил и-459,67 °F. В этих условиях молекулы перестают двигаться и застывают в узлах кристаллической решетки. Но достичь такого температурного режима невозможно ни на планете Земля, ни во всей Вселенной, ни даже в лаборатории.
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Зарегистрируйтесь и примите участие в розыгрыше 8 курсов.

Заключение
Агрегатное состояние газа изучали многие выдающиеся физики и химики: Авогадро, Бойль, Гей-Люссак, Клайперон, Менделеев, Ле-Шателье. Ученые сформулировали законы, объясняющие поведение газообразных веществ в химических реакциях, при изменении внешних условий. Открытые закономерности не только вошли в школьные и вузовские учебники физики и химии. Многие химические производства основаны на знаниях о поведении и свойствах веществ, находящихся в разных агрегатных состояниях.
Зимой вода на поверхности озер и рек замерзает, превращаясь в лед. Подо льдом вода остается жидкой (рис. 76). Здесь одновременно существуют два различных состояния воды — твердое (лед) и жидкое (вода). Существует и третье состояние воды — газообразное: невидимый водяной пар находится в окружающем нас воздухе. На примере воды мы видим, что вещества могут находиться в трех агрегатных состояниях — твердом, жидком и газообразном
.
Жидкую ртуть можно увидеть в резервуаре термометра. Над поверхностью ртути находятся ее пары, которые представляют собой газообразное состояние ртути. При температуре -39 °С ртуть замерзает, переходя в твердое состояние.
Кислород в окружающем нас воздухе представляет собой газ. Но при температуре -193 °С он превращается в жидкость. Охладив эту жидкость до -219 °С, мы получим твердый кислород.
И наоборот, железо в обычных условиях твердое. Однако при температуре 1535 °С железо плавится и превращается в жидкость. Над расплавленным железом будет находиться газ — пар из атомов железа.
Свойства вещества в различных агрегатных состояниях различны.
Твердое тело
в обычных условиях трудно сжать или растянуть. В отсутствие внешних воздействий оно сохраняет свою форму и объем.
Жидкость
легко меняет свою форму. В обычных условиях она принимает форму сосуда, в котором находится (рис. 77). Но в состоянии невесомости (например, на орбитальной космической станции) жидкость характеризуется своей собственной — сферической — формой. Сферическую форму (форму шарика) имеют и маленькие дождевые капельки.
Свойство жидкости легко изменять свою форму учитывают, когда изготавливают посуду из расплавленного стекла (рис. 78). 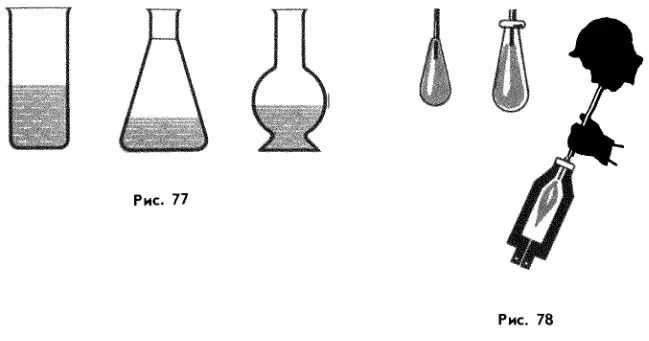
Форму жидкости изменить легко, но объем ее изменить трудно. Сохранилось описание одного исторического опыта, в котором воду пробовали сжать таким способом. Ее налили в свинцовый шар и шар запаяли, чтобы вода не могла выливаться при сжатии. После этого ударили по свинцовому шару тяжелым молотом. И что же? Вода не сжалась вместе с шаром, а просочилась сквозь его стенки.
Итак, жидкости легко меняют свою форму, но сохраняют свой объем.
Газ
не имеет своего собственного объема и не обладает собственной формой. Он всегда заполняет всю предоставленную ему емкость.
Чтобы исследовать свойства газов, необязательно располагать газом, имеющим цвет. Воздух, например, бесцветен, и мы его не видим. Но при быстром движении, находясь у окна автомобиля или поезда, а также когда дует ветер, мы замечаем присутствие воздуха вокруг нас. Его можно обнаружить и при помощи опытов.
Опустим в воду перевернутый вверх дном стакан — вода не заполнит стакан, так как в нем останется воздух. Если опускать в воду воронку, соединенную резиновым шлангом со стеклянной трубкой (рис. 79), то воздух начнет выходить из нее наружу. Объем газа изменить нетрудно. Нажав на резиновый мяч, мы заметно уменьшим объем воздуха, находящегося в мяче.
Попав в какой-нибудь сосуд или помещение, газ заполняет их целиком, принимая как их форму, так и объем.
1. В каких трех агрегатных состояниях может находиться любое вещество? Приведите примеры. 2. Тело сохраняет свой объем, но легко меняет форму. В каком состоянии находится это тело? 3. Тело сохраняет свою форму и объем. В каком состоянии находится это тело? 4. Что вы можете сказать о форме и объеме газа?




























